Aktif maddeler: Kalsitriol
DIFIX 0.25 mikrogram yumuşak kapsül
DIFIX 0,50 mikrogram yumuşak kapsül
Endikasyonları Difix neden kullanılır? Bu ne için?
FARMAKOTERAPÖTİK KATEGORİ
Aktif D Vitamini.
TEDAVİ ENDİKASYONLARI
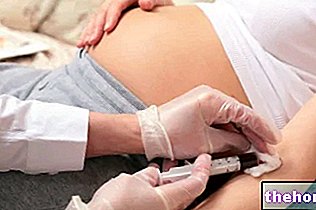
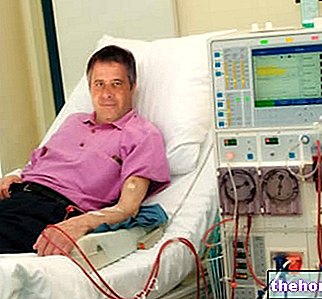
Kronik böbrek yetmezliği olan hastalarda, özellikle hemodiyaliz uygulananlarda renal osteodistrofi.
Hem idiyopatik hem de cerrahi hipoparatiroidizm.
Psödohipoparatiroidizm.
D vitaminine dirençli hipofosfatemik raşitizm.
Sözde bağımlı D vitamini ailesel raşitizm.
Menopoz sonrası osteoporoz: Ayırıcı tanı, multipl miyelom ve tümör osteolizi gibi DIFIX tedavisinin endike olmadığı benzer iskelet semptomları olan durumları dikkatle dışlamalıdır.
Kontrendikasyonlar Difix kullanılmamalıdır
DIFIX kontrendikedir:
- Kalsitriole (veya aynı sınıftaki ilaçlara) ve yardımcı maddelerden herhangi birine karşı aşırı duyarlılığı olan hastalarda
- hiperkalsemi ile ilişkili tüm bozukluklarda
- D vitamini toksisitesi kanıtı varsa
Kullanım Önlemleri Difix kullanmadan önce bilmeniz gerekenler
Kalsitriol tedavisi ile hiperkalsemi gelişimi arasında yakın bir ilişki vardır.
Hiperkalsemi, diyet değişikliklerinden (örneğin artan süt ürünleri tüketimi) veya kalsiyum preparatlarının kontrolsüz alımından kaynaklanan kalsiyum alımında keskin bir artışla tetiklenebilir.
Hastalara ve ailelerine reçete edilen diyete sıkı sıkıya uymaları tavsiye edilmeli ve hiperkalsemi semptomlarını nasıl tanıyacakları konusunda bilgilendirilmelidirler.
Serum kalsiyum seviyeleri normal konsantrasyonun (9-11mg / 100ml veya 2250-2750μmol / L) 1mg / 100ml (250μmol / L) üzerine çıkarsa veya serum kreatinin seviyesi 120μmol / L'ye yükselirse, DIFIX tedavisi kesilmelidir. hemen normal kalsiyum konsantrasyonları geri gelene kadar (bkz. Pozoloji ve uygulama yöntemi bölümü).
Ameliyat geçirmiş olanlar gibi hareketsiz hastalar özellikle hiperkalsemi riski altındadır.
Kalsitriol, inorganik fosfatın serum seviyelerini yükseltir.
Bu hipofosfatemili hastalarda arzu edilirken, ektopik kalsifikasyon riskinden dolayı böbrek yetmezliği olan hastalarda dikkatli olunmalıdır.
Bu durumlarda, uygun fosfat bağlayıcı ajanların oral yoldan uygulanması ve düşük fosfatlı bir diyet ile plazma fosfat seviyesi normal bir konsantrasyonda (2-5mg / 100ml veya 0.65-1.62mmol / l) tutulmalıdır.
Kalsiyum değeri ile fosfat değeri (Ca X P) çarpılarak elde edilen sonuç 70 mg2/dl2'yi geçmemelidir.
DIFIX ile tedavi edilen D vitamini direnci raşitizmi (ailesel hipofosfatemi) olan hastalar oral fosfat tedavisine devam etmelidir.
Bununla birlikte, fosfatın bağırsak absorpsiyonunun olası bir uyarımı dikkate alınmalıdır, çünkü bu etki buna olan ek ihtiyacı değiştirebilir.
Kalsitriol, D vitamininin mevcut en etkili metaboliti olduğundan, DIFIX ile tedavi sırasında başka hiçbir D vitamini preparatı reçete edilmemelidir, böylece hipervitaminoz D gelişiminin önlenmesi sağlanır.
Hasta ergokalsiferol (D2 vitamini) tedavisinden kalsitriole geçerse, kan ergokalsiferol konsantrasyonunun başlangıç değerine dönmesi birkaç ay sürebilir (bkz. Doz aşımı bölümü).
DIFIX alan normal böbrek fonksiyonu olan hastalar dehidratasyondan kaçınmalıdır.
Yeterli sıvı alımı her zaman sağlanmalıdır.
Normal böbrek fonksiyonu olan hastalarda, kronik hiperkalsemi serum kreatinin artışı ile ilişkili olabilir.
Alkalin fosfataz değerlerindeki düşüş genellikle hiperkalseminin başlangıcını öngörür ve bu nedenle hiperkalseminin habercisi olabilir.
Menopoz sonrası osteoporozlu hastalarda, tedaviye başlamadan önce ve DIFIX ile tedavi sırasında düzenli aralıklarla böbrek fonksiyonunun ve kan kalsiyumunun dikkatle izlenmesi önemlidir.
DIFIX'in 3 yaşın altındaki çocuklarda güvenliği ve etkinliği henüz belirlenmemiştir, bu nedenle kullanımı doktorun görüşüne göre mutlak gereklilik durumlarında kullanılmalıdır.İlaç, çölyak hastalığı olan kişilerde kontrendike değildir. .
Bu ilacı çocukların erişemeyeceği bir yerde saklayın.
Etkileşimler Hangi ilaçlar veya yiyecekler Difix'in etkisini değiştirebilir?
"Reçetesizler de dahil olmak üzere yakın zamanda başka ilaçlar aldıysanız, doktorunuza veya eczacınıza söyleyiniz."
Kalsitriol, D vitamininin mevcut en etkili metaboliti olduğundan, kalsitriol ile tedavi sırasında başka hiçbir D vitamini preparatı reçete edilmemelidir, böylece hipervitaminoz D gelişiminin önlenmesi sağlanır. ergokalsiferolün kan konsantrasyonunun başlangıç değerine dönmesi birkaç ay sürebilir.
DIFIX ile tedavi sırasında olası ek etkilerden ve hiperkalsemiden kaçınmak için D vitamini ve türevlerinin farmakolojik dozlarından kaçınılmalıdır.
Reçete edilen diyetle ilgili talimatlar, özellikle kalsiyum takviyeleri ile ilgili olarak kesinlikle takip edilmelidir ve ek kalsiyum içeren preparatların kontrolsüz alımından kaçınılmalıdır.Bir tiyazid diüretik ile birlikte tedavi, hiperkalsemi riskini artırır.Gerektiğinde kalsitriol dozu Bu hastalarda hiperkalsemi kardiyak aritmilere neden olabileceğinden dijital tedavi alan hastalarda doğru bir şekilde belirlenmelidir (kullanım önlemleri bölümüne bakınız).
Kalsiyum emilimini artıran D vitamini analogları ile tam tersine onu engelleyen kortikosteroidler arasında fonksiyonel bir antagonizma ilişkisi vardır.
Magnezyum içeren ilaçlar (antasitler gibi) hipermagnezemiye neden olabilir ve bu nedenle kronik böbrek diyalizindeki hastalar tarafından DIFIX tedavisi sırasında alınmamalıdır.
DIFIX ayrıca fosfatın bağırsakta, böbreklerde ve kemiklerde taşınması üzerinde de bir etkiye sahip olduğundan, fosfat bağlayıcı ajanların dozu serum fosfat konsantrasyonuna göre ayarlanmalıdır (normal değerler: 2-5 mg / 100ml veya 0.65-1.62 mmol). /L).
D vitamini direnci (ailesel hipofosfatemi) nedeniyle raşitizm hastaları oral fosfat tedavisine devam etmelidir. Bununla birlikte, bu etki ek ihtiyacı değiştirebileceğinden, fosfatın bağırsak emiliminin olası bir uyarımı dikkate alınmalıdır.
Fenitoin veya fenobarbital gibi enzim indükleyicilerin uygulanması metabolizmanın artmasına ve dolayısıyla serum kalsitriol düzeylerinin düşmesine neden olabilir. Bu nedenle, bu ilaçlar birlikte verilirse yüksek dozlarda kalsitriol gerekebilir.
Kolestiramin ve sevelamer dahil safra asitlerini tutan maddeler, yağda çözünen vitaminlerin bağırsak emilimini azaltabilir ve böylece kalsitriolün bağırsak emilimini değiştirebilir.
Uyarılar Şunları bilmek önemlidir:
Hamilelik, emzirme ve doğurganlık
"Herhangi bir ilacı almadan önce doktorunuza veya eczacınıza danışınız".
Gebelik
Supravalvüler aort stenozu, hamile tavşanlara neredeyse ölümcül dozlarda D vitamini uygulandığında tavşan fetüslerinde meydana geldi. D vitamininin çok yüksek dozlarda bile insanlarda teratojenik olduğuna dair bir kanıt yoktur.DIFIX sadece hamilelikte yararları fetüs için potansiyel riskten ağır basıyorsa kullanılmalıdır.Gebe kadınlarda ürün, gerçek vakalarda uygulanmalıdır. doktorun doğrudan gözetimi altında gereklidir.
Besleme zamanı
Eksojen kalsitriolün anne sütüne geçtiği varsayılabilir. Annede hiperkalsemi olasılığı ve bebeklerde DIFIX'in advers reaksiyonları göz önüne alındığında, anne ve bebeğin serum kalsiyum düzeylerinin izlenmesi şartıyla anneler DIFIX alırken emzirebilir.
Araç ve makine kullanma yeteneği üzerindeki etkiler
Bildirilen advers olayların farmakodinamik profiline dayanarak, bu ürünün güvenli olduğu veya makine kullanımı ve araç kullanma yeteneği üzerindeki olumsuz etkisinin olası olmadığı varsayılmaktadır.
Yardımcı maddelerin bazıları hakkında önemli bilgiler
DIFIX kapsülleri sorbitol içerir. Eğer daha önceden doktorunuz tarafından bazı şekerlere karşı intoleransınız olduğu söylenmişse, bu tıbbi ürünü almadan önce doktorunuzla temasa geçiniz.
Dozaj ve kullanım yöntemi Difix nasıl kullanılır: Dozaj
DIFIX'in optimal günlük dozu, kalsiyum değerleri temelinde her hastada dikkatli bir şekilde belirlenmelidir.
Renal osteodistrofi: Tedavinin etkinliği, aynı anda kalsiyum alımı ile belirlenir: yetişkinlerde ek kalsiyum alımı günde 600-1000 mg olmalıdır.
DIFIX'in önerilen başlangıç dozu günde 0.25 mikrogramdır; Kalsiyumu normal veya çok az azalmış hastalarda 2 günde bir 0.25 mikrogramlık başlangıç dozları yeterlidir. 2-4 hafta sonra klinik tablo ve biyokimyasal parametrelerde herhangi bir iyileşme gözlenmezse, DIFIX dozu 2-4 haftalık aralıklarla günde 0.25 mikrogram artırılmalıdır.
Bu süre içinde haftada en az iki kez kalsiyum düzeyi kontrol edilmeli ve hiperkalsemi saptanırsa DIFIX uygulaması ve kalsiyum düzeyi normal sınırlara gelene kadar ek kalsiyum uygulaması derhal durdurulmalıdır.
Tedavi daha sonra bir öncekinden 0.25 mcg daha düşük bir günlük dozla devam ettirilecektir.
Yukarıda belirtilen yöntemlere göre belirlenecek olan optimal günlük DIFIX dozu, çoğu hastada 0,5 mcg ile 1 mcg arasındadır. Barbitüratların veya antikonvülzanların birlikte uygulanması durumunda daha yüksek dozlar gerekli olabilir.
Hipoparatiroidizm ve raşitizm: Önerilen DIFIX dozu, sabahları uygulanmak üzere günde 0.25 mikrogramdır.Klinik ve biyokimyasal parametrelerde herhangi bir iyileşme görülmezse, doz 2-4 haftada bir arttırılabilir.Bu aralık sırasında, kalsiyum haftada en az iki kez belirlenmelidir.
Hipoparatiroidizmi olan hastalarda bazen malabsorpsiyon sendromu görülebilir; bu durumlarda daha yüksek dozlarda DIFIX gerekebilir.
Postmenopozal osteoporoz: Günde iki kez 0,5 mikrogram ile başlanması ve eğer kalsiyum seviyelerinde önemli bir değişiklik yoksa bu doz ile devam edilmesi önerilir.
Renal osteodistrofiden farklı olarak, ek bir kalsiyum kaynağından kaçınmak kesinlikle gereklidir.
Tedavinin ilk ayında, kalsiyum haftada en az bir kez kontrol edilmelidir. Hiperkalsemi (> 11.5 mg / 100 ml) durumunda, DIFIX uygulaması normokalsemi düzelene kadar askıya alınmalıdır.
Hekimin görüşüne göre kalsitonin ile ilişki mümkündür (özellikle yüksek devirli osteoporoz durumunda).
Genel bilgi: Optimal pozoloji belirlendikten sonra ayda bir kez kan kalsiyumunun kontrolü yeterlidir.
Serum kalsiyum seviyesinin normal değerleri 100 ml'de 1 mg (mg 9-11 / 100 ml) aşması durumunda, DIFIX dozu önemli ölçüde azaltılmalı veya normal kan kalsiyumu geri gelene kadar tedavi durdurulmalıdır.
Serum kalsiyum değerlerinin hızlı normalleşmesini desteklemek için renal osteodistrofi, hipoparatiroidizm ve raşitizm tedavisi için sağlanan ek kalsiyum uygulaması da kesilebilir. Diyetle alınan kalsiyum miktarı da sınırlandırılmalıdır.
Hiperkalsemi döneminde serum kalsiyum ve fosfor düzeylerinin günlük olarak kontrol edilmesi gerekir. Normal değerler geri yüklendiğinde, DIFIX ile tedaviye öncekinden 0.25 mikrogramlık daha düşük bir günlük dozda devam edilebilir.
Pediatrik popülasyon
Kalsitriol kapsüllerinin çocuklarda güvenliliği ve etkililiği, doz önerilerinde bulunmak için yeterince araştırılmamıştır Pediyatrik hastalarda kalsitriol kapsülleri hakkında sınırlı veri mevcuttur.
Doz aşımı Çok fazla Difix aldıysanız ne yapmalısınız?
Herhangi bir D vitamini formunun aşırı dozu ciddi belirtilere bile neden olur.
Aşırı dozda D vitamini veya metabolitlerinin neden olduğu hiperkalsemi de acil tedavi gerektirebilir.
Olası kalsifikasyonların anatomik bölgelerinin radyografik muayenesi erken tanı için faydalı olabilir.
Asemptomatik hiperkalseminin tedavisi: (Doz, uygulama yöntemi ve zamanı ile ilgili bölüme bakınız).
Difix doz aşımı hiperkalsemiye ve bazı durumlarda hiperkalsiüriye neden olabileceğinden, doz ayarlama aşamasında kalsiyum en az haftada iki kez verilmelidir. Optimal günlük doz belirlendikten sonra, aylık kan kalsiyum kontrolü yeterlidir.
Kalsitriol, D vitamininin bir türevi olduğundan, doz aşımı belirtileri D vitamini ile aynıdır. DIFIX ile birlikte yüksek dozda kalsiyum ve fosfat alımı benzer belirtilere neden olabilir. fosfatemi (Ca XP) 70mg2/dl2'yi geçmemelidir Diyaliz hastasında yüksek düzeyde kalsiyum hiperkalsemi gelişimine katkıda bulunabilir.
D vitamini zehirlenmesinin akut belirtileri: anoreksi, baş ağrısı, kusma, kabızlık.
Kronik semptomlar: distrofi (zayıflık, kilo kaybı), duyusal bozukluklar, susuzluk, poliüri, dehidratasyon, apati, bodur büyüme ve idrar yolu enfeksiyonlarının eşlik ettiği olası ateşli durumlar.
Hiperkalsemi renal korteks, miyokard, akciğerler ve pankreasta metastatik kalsifikasyona yol açabilir.
Kazara aşırı dozun tedavisinde aşağıdaki ihtiyati tedbirler dikkate alınmalıdır: daha fazla emilimi önlemek için hemen gastrik lavaj veya kusma indüksiyonu.
Dışkı atılımını kolaylaştırmak için sıvı parafin uygulanabilir.
Serum kalsiyumunun tekrarlanan ölçümleri tavsiye edilir. Yüksek serum kalsiyum seviyeleri devam ederse, fosfatlar ve kortikosteroidler uygulanabilir ve yeterli diürez elde etmek için önlemler alınabilir.
Yüksek seviyelere (> 3.2 mmol / L) kadar hiperkalsemi, özellikle kandaki fosfat seviyeleri normalse veya böbrek fonksiyon bozukluğu nedeniyle yükselmişse, böbrek yetmezliğine yol açabilir.
"Yanlışlıkla yutulması/aşırı dozda DIFIX alınması durumunda derhal doktorunuza veya en yakın hastaneye başvurunuz".
Yan Etkiler Difix'in yan etkileri nelerdir?
Tüm ilaçlar gibi, herkeste görülmese de DIFIX yan etkilere neden olabilir.
Klinik çalışmalar
Aşağıda listelenen advers reaksiyonlar, klinik denemeler sırasında ve pazarlama sonrası aşamada kalsitriol ile olan deneyimi yansıtmaktadır.
Hiperkalsemi, en sık bildirilen advers reaksiyondur.Aşağıda listelenen istenmeyen etkilerin sıklıkları, aşağıdaki kurala göre tanımlanmıştır:
- Çok yaygın: 10 kullanıcıda 1'den fazla kullanıcıyı etkiler
- Yaygın: 100'de 1 ila 10 kullanıcıyı etkiler
- Yaygın olmayan: 1000 kullanıcıdan 1 ila 10'unu etkiler
- Seyrek: 10.000'de 1 ila 10 kullanıcıyı etkiler
- Çok seyrek: 10.000'de 1'den az kullanıcıyı etkiler
- Bilinmiyor: mevcut verilerden sıklık tahmin edilemiyor
Çok yaygın:
- hiperkalsemi
Yaygın:
- Baş ağrısı, karın ağrısı, bulantı, döküntü, idrar yolu enfeksiyonu
Yaygın olmayan:
- İştah azalması, kusma, kan kreatinin artışı
Bilinmeyen:
- Aşırı duyarlılık, ürtiker, polidipsi, dehidratasyon, düşük ağırlık, apati, kas zayıflığı, duyu bozukluğu, kabızlık, üst karın ağrısı, eritem, kaşıntı, büyüme geriliği, poliüri, kalsinoz, ateş, susuzluk
Kalsitriol D vitamini aktivitesini uyguladığından, çok fazla D vitamini alındığında görülenlere benzer yan etkiler ortaya çıkabilir, örneğin hiperkalsemik sendrom veya kalsiyum intoksikasyonu (hiperkalseminin şiddetine ve süresine bağlı olarak) (bkz. uygulama ve Kullanım Önlemleri bölümü).
Ara sıra akut semptomlar iştah azalması, baş ağrısı, bulantı, kusma, ağız kuruluğu, karın ağrısı veya üst karın ağrısı, kabızlık, kemik ve kas ağrısını içerir.
Kalsitriolün kısa biyolojik yarı ömrü nedeniyle, farmakokinetik çalışmalar, yüksek serum kalsiyum düzeylerinin tedaviyi bıraktıktan sonraki birkaç gün içinde normale döndüğünü, yani D3 vitamini preparatları ile yapılan tedavilere göre çok daha hızlı olduğunu göstermiştir.
Kronik etkiler arasında kas zayıflığı, kilo kaybı, duyu bozuklukları, ateş, susuzluk, polidipsi, poliüri, dehidratasyon, apati, büyüme geriliği, idrar yolu enfeksiyonları sayılabilir.
> 6mg / 100ml veya 1.9mmol / l'lik hiperkalsemi ve hiperfosfatemi ile birlikte kalsinozis oluşabilir; bu fenomen radyografik olarak görülebilir.
Yatkınlığı olan kişilerde deri döküntüsü, eritem, kaşıntı ve ürtiker gibi aşırı duyarlılık reaksiyonları ortaya çıkabilir.
Laboratuvar Anomalileri
Normal böbrek fonksiyonu olan hastalarda, kronik hiperkalsemi, kan kreatininde bir artış ile ilişkili olabilir.
Pazarlama sonrası
Tüm endikasyonlar için 15 yıllık bir süre boyunca izlenen DIFIX'in klinik kullanımında bildirilen yan etkilerin sayısı çok düşüktür ve hiperkalsemi dahil herhangi bir tek etkinin insidans oranı %0,001 veya daha azdır.
Kullanma talimatında yer alan talimatlara uyulması, istenmeyen etki riskini azaltır.
Yan etkilerin raporlanması
Herhangi bir yan etki yaşarsanız, doktorunuzla veya eczacınızla konuşun.Bu kullanma talimatında listelenmeyen olası yan etkiler de buna dahildir. Yan etkileri doğrudan İtalyan İlaç Ajansı, www.agenziafarmaco.it/it/responsabili web sitesi aracılığıyla da bildirebilirsiniz. Yan etkileri bildirerek, bu ilacın güvenliği hakkında daha fazla bilgi sağlamaya yardımcı olabilirsiniz.
Son Kullanma ve Saklama
Son kullanma tarihi: Paketin üzerinde yazılı olan son kullanma tarihine bakın.
Son kullanma tarihi, bozulmamış ve doğru şekilde saklanmış ambalajdaki ürünü ifade eder.
Uyarı: Paket üzerinde belirtilen son kullanma tarihinden sonra ilacı kullanmayınız.
30 ° C'nin altındaki bir sıcaklıkta saklayın
İlaçlar atık su veya evsel atıklar yoluyla atılmamalıdır.Artık kullanmadığınız ilaçları nasıl atacağınızı eczacınıza sorunuz.Bu çevrenin korunmasına yardımcı olacaktır.
Bu ilacı çocukların erişemeyeceği ve göremeyeceği bir yerde saklayın.
Diğer bilgiler
KOMPOZİSYON
Her 0.25 mikrogram kapsül şunları içerir:
Aktif madde: Kalsitriol 0.25 mikrogram.
Yardımcı maddeler: butilhidroksianisol, butilhidroksitoluen, orta zincirli trigliseritler, jelatin, gliserol, %85 sorbitol çözeltisi, sorbitanlar ve mannitol, etil-p-oksibenzoat sodyum tuzu (E 215), propil-p-oksibenzoat sodyum tuzu (E 217) , titanyum dioksit (E 171).
Her 0,50 mikrogram kapsül şunları içerir:
Aktif madde: Kalsitriol 0.50 mikrogram.
Yardımcı maddeler: butilhidroksianisol, butilhidroksitoluen, orta zincirli trigliseritler, jelatin, gliserol, %85 sorbitol çözeltisi, sorbitanlar ve mannitol, etil-p-oksibenzoat sodyum tuzu (E 215), propil-p-oksibenzoat sodyum tuzu (E 217) , titanyum dioksit (E 171), kantaksantin %10 (E 161).
FARMASÖTİK FORM VE İÇERİĞİ
DIFIX 0.25 mikrogram yumuşak kapsül
- 30 kapsüllük kutu.
DIFIX 0,50 mikrogram yumuşak kapsül
- 30 kapsüllük kutu.
Kaynak Paket Broşürü: AIFA (İtalyan İlaç Ajansı). Ocak 2016'da yayınlanan içerik. Mevcut bilgiler güncel olmayabilir.
En güncel sürüme erişmek için AIFA (İtalyan İlaç Ajansı) web sitesine erişmeniz önerilir. Sorumluluk reddi ve faydalı bilgiler.
01.0 TIBBİ ÜRÜNÜN ADI
DIFIX YUMUŞAK KAPSÜLLER
02.0 KALİTATİF VE KANTİTATİF BİLEŞİM
Her 0.25 mcg kapsül şunları içerir:
Aktif madde: kalsitriol 0.25 mcg.
Yardımcı maddeler: sorbitol içerir
"Yardımcı maddelerin tam listesi için bkz. bölüm 6.1".
Her 0,50 mcg kapsül şunları içerir:
Aktif madde: kalsitriol 0.50 mcg.
Yardımcı maddeler: sorbitol içerir
"Yardımcı maddelerin tam listesi için bkz. bölüm 6.1".
03.0 FARMASÖTİK FORM
Yumuşak kapsüller
04.0 KLİNİK BİLGİLER
04.1 Terapötik endikasyonlar
Kronik böbrek yetmezliği olan hastalarda, özellikle hemodiyaliz uygulananlarda renal osteodistrofi.
Hem idiyopatik hem de cerrahi hipoparatiroidizm.
Psödohipoparatiroidizm.
D vitaminine dirençli hipofosfatemik raşitizm.
Sözde bağımlı D vitamini ailesel raşitizm.
Menopoz sonrası osteoporoz: Ayırıcı tanı, multipl miyelom ve tümör osteolizi gibi DIFIX tedavisinin endike olmadığı benzer iskelet semptomları olan durumları dikkatle dışlamalıdır.
04.2 Pozoloji ve uygulama yöntemi
DIFIX'in optimal günlük dozu, kalsiyum değerleri temelinde her hastada dikkatli bir şekilde belirlenmelidir.
Renal osteodistrofi: Tedavinin etkinliği, aynı anda kalsiyum alımı ile belirlenir: yetişkinlerde ek kalsiyum alımı günde 600-1000 mg olmalıdır.
DIFIX'in önerilen başlangıç dozu günde 0.25 mcg'dir; kalsiyumu normal veya çok az azalmış hastalarda 2 günde bir 0.25 mcg başlangıç dozları yeterlidir. Klinik tablo ve biyokimyasal parametreler, DIFIX dozu günde 0.25 mikrogram artırılmalıdır. Bu süre zarfında haftada en az iki kez kalsiyum kontrolü yapılmalı ve hiperkalsemi bulunursa DIFIX uygulamasına ve ilave kalsiyuma "kalsiyum seviyesi normal sınırlar içinde olana kadar" derhal ara verilmelidir.
Tedavi daha sonra bir öncekinden 0.25 mcg daha düşük bir günlük dozla devam ettirilecektir.
Yukarıda belirtilen yöntemlere göre belirlenecek olan optimal günlük DIFIX dozu, "çoğu hastada 0,5 mcg ile 1 mcg arasındadır. Barbitüratlar veya antikonvülzanların birlikte uygulanması durumunda daha yüksek dozlar gerekli olabilir.
Hipoparatiroidizm ve raşitizm: Önerilen DIFIX dozu, sabahları uygulanmak üzere günde 0.25 mikrogramdır.Klinik ve biyokimyasal parametrelerde herhangi bir iyileşme görülmezse, doz 2-4 haftada bir arttırılabilir. Bu aralık sırasında, kalsiyum haftada en az iki kez belirlenmelidir.
Hipoparatiroidizmi olan hastalarda bazen bir malabsorpsiyon sendromu gözlenebilir ve bu durumlarda daha yüksek dozlarda DIFIX gerekebilir.
Postmenopozal osteoporoz: Günde iki kez 0,5 mikrogram uygulamasıyla başlanması ve kalsiyum seviyelerinde önemli bir değişiklik yoksa bu dozla devam edilmesi önerilir.
"Renal osteodistrofi"den farklı olarak, ek bir kalsiyum alımından kaçınılmalıdır.
Tedavinin ilk ayında, kalsiyum haftada en az bir kez kontrol edilmelidir. Hiperkalsemi (> 11.5 mg / 100 ml) durumunda, DIFIX uygulaması normokalsemi düzelene kadar askıya alınmalıdır.
Hekimin görüşüne göre kalsitonin ile ilişki "mümkün"dür (özellikle yüksek devirli osteoporoz durumunda).
Genel bilgi: Optimal dozaj belirlendikten sonra ayda bir kalsiyum kontrolü yeterlidir.
Serum kalsiyum seviyesinin normal değerleri 100 ml'de 1 mg (mg 9/11/100 ml) aşması durumunda, DIFIX dozu önemli ölçüde azaltılmalı veya normal kan kalsiyumu geri gelene kadar tedavi durdurulmalıdır.
Serum kalsiyum değerlerinin hızlı bir şekilde normale dönmesini sağlamak için renal osteodistrofi, hipoparatiroidizm ve raşitizm tedavisi için sağlanan ek kalsiyum uygulamasına son vermek de mümkündür.Diyette verilen kalsiyum miktarı sınırlı olmalıdır.
Hiperkalsemi döneminde serum kalsiyum ve fosfor seviyelerinin günlük olarak kontrol edilmesi gerekir.Normal değerlere ulaşıldığında, DIFIX ile tedaviye öncekine kıyasla 0.25 mcg'den daha düşük bir günlük doz ile devam edilebilir. .
Pediatrik popülasyon
Kalsitriol kapsüllerinin çocuklarda güvenliliği ve etkililiği, doz önerilerinde bulunmak için yeterince araştırılmamıştır Pediyatrik hastalarda kalsitriol kapsülleri hakkında sınırlı veri mevcuttur.
04.3 Kontrendikasyonlar
DIFIX kontrendikedir:
• kalsitriole (veya aynı sınıftaki ilaçlara) ve yardımcı maddelerden herhangi birine karşı aşırı duyarlılığı olduğu bilinen hastalarda
• hiperkalsemi ile ilişkili tüm bozukluklarda
• D vitamini toksisitesi kanıtı varsa
04.4 Özel uyarılar ve uygun kullanım önlemleri
Kalsitriol tedavisi ile hiperkalsemi gelişimi arasında yakın bir ilişki vardır.
Hiperkalsemi, diyet değişikliklerinden (örneğin artan süt ürünleri tüketimi) veya kalsiyum preparatlarının kontrolsüz alımından kaynaklanan kalsiyum alımında keskin bir artışla tetiklenebilir.
Hastalara ve ailelerine reçete edilen diyete sıkı sıkıya uymaları tavsiye edilmeli ve hiperkalsemi semptomlarını nasıl tanıyacakları konusunda bilgilendirilmelidirler. Serum kalsiyum seviyeleri normal konsantrasyonun (9-11mg/100ml veya 2250-2750mcmol/L) üzerine 1mg/100ml (250mcmol/L) yükselir yükselmez veya serum kreatinin seviyesi >120mcmol/l'ye yükselir yükselmez, DIFIX ile tedavi durdurulmalıdır. hemen normal kalsiyum konsantrasyonları geri gelene kadar (bkz. bölüm 4.2 Pozoloji ve uygulama yöntemi).
Ameliyat geçirmiş olanlar gibi hareketsiz hastalar özellikle hiperkalsemi riski altındadır.
Kalsitriol, inorganik fosfatın serum seviyelerini yükseltir.
Bu hipofosfatemili hastalarda arzu edilirken, ektopik kalsifikasyon riskinden dolayı böbrek yetmezliği olan hastalarda dikkatli olunmalıdır.
Bu durumlarda, uygun fosfat bağlayıcı ajanların oral yoldan uygulanması ve düşük fosfatlı bir diyet ile plazma fosfat seviyesi normal bir konsantrasyonda (2-5mg / 100ml veya 0.65-1.62mmol / l) tutulmalıdır.
Kalsiyum değeri ile fosfat değeri (Ca X P) çarpılarak elde edilen sonuç 70 mg2/dl2'yi geçmemelidir.
DIFIX ile tedavi edilen D vitamini direnci raşitizmi (ailesel hipofosfatemi) olan hastalar oral fosfat tedavisine devam etmelidir.
Bununla birlikte, bu etki ek ihtiyacı değiştirebileceğinden, fosfatın bağırsak emiliminin olası bir uyarımı dikkate alınmalıdır.
Kalsitriol, D vitamininin mevcut en etkili metaboliti olduğundan, DIFIX ile tedavi sırasında başka hiçbir D vitamini preparatı reçete edilmemelidir, böylece hipervitaminoz D gelişiminin önlenmesi sağlanır.
Hasta ergokalsiferol (D2 vitamini) tedavisinden kalsitriole geçerse, kan ergokalsiferol konsantrasyonunun başlangıç değerine dönmesi birkaç ay sürebilir (bkz. bölüm 4.9 Doz aşımı).
DIFIX alan normal böbrek fonksiyonu olan hastalar dehidratasyondan kaçınmalıdır.
Yeterli sıvı alımı her zaman sağlanmalıdır.
Normal böbrek fonksiyonu olan hastalarda, kronik hiperkalsemi serum kreatinin artışı ile ilişkili olabilir.
Alkalin fosfataz değerlerindeki düşüş genellikle hiperkalseminin başlangıcını öngörür ve bu nedenle hiperkalseminin habercisi olabilir.
Menopoz sonrası osteoporozlu hastalarda, tedaviye başlamadan önce ve DIFIX ile tedavi sırasında düzenli aralıklarla böbrek fonksiyonunun ve kan kalsiyumunun dikkatle izlenmesi önemlidir.
DIFIX'in 3 yaşın altındaki çocuklarda güvenliliği ve etkinliği henüz belirlenmemiştir, bu nedenle hekimin görüşüne göre kullanımı mutlak gereklilik durumlarında kullanılmalıdır.
DIFIX kapsülleri sorbitol içerir. Nadir kalıtsal fruktoz intoleransı sorunları olan hastalar bu ilacı almamalıdır.
04.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim biçimleri
Kalsitriol, D vitamininin mevcut en etkili metaboliti olduğundan, kalsitriol ile tedavi sırasında başka hiçbir D vitamini preparatı reçete edilmemelidir, böylece hipervitaminoz D gelişiminin önlenmesi sağlanır.Hasta ergokalsiferolden (D2 vitamini) kalsitriole geçerse ergokalsiferol kan konsantrasyonunun taban çizgisine dönmesi için birkaç ay.
DIFIX ile tedavi sırasında olası ek etkilerden ve hiperkalsemiden kaçınmak için D vitamini ve türevlerinin farmakolojik dozlarından kaçınılmalıdır.
Kalsiyum takviyeleri başta olmak üzere, reçete edilen diyet rejimindeki talimatlara kesinlikle uyulmalı ve ilave kalsiyum içeren müstahzarların kontrolsüz alımından kaçınılmalıdır.
Bir tiyazid diüretik ile eşzamanlı tedavi, hiperkalsemi riskini artırır. Hiperkalsemi, kardiyak aritmilere neden olabileceğinden, dijital tedavi altındaki hastalarda kalsitriol dozu dikkatli bir şekilde belirlenmelidir (bkz. bölüm 4.4 Özel kullanım uyarıları ve önlemleri).
Kalsiyum emilimini artıran D vitamini analogları ile tam tersine onu engelleyen kortikosteroidler arasında fonksiyonel bir antagonizma ilişkisi vardır.
Magnezyum içeren ilaçlar (örneğin antasitler) hipermagnezemiye neden olabilir ve bu nedenle kronik böbrek diyalizi hastaları tarafından DIFIX ile tedavi sırasında alınmamalıdır.
DIFIX ayrıca fosfatın bağırsakta, böbreklerde ve kemiklerde taşınması üzerinde de bir etkiye sahip olduğundan, fosfat bağlayıcı ajanların dozu serum fosfat konsantrasyonuna göre ayarlanmalıdır (normal değerler: 2-5 mg / 100 ml veya 0.65-1.62). mmol / l).
D vitamini direnci (ailesel hipofosfatemi) nedeniyle raşitizm hastaları oral fosfat tedavisine devam etmelidir. Bununla birlikte, fosfatın bağırsak absorpsiyonunun olası bir uyarımı dikkate alınmalıdır, çünkü bu etki buna olan ek ihtiyacı değiştirebilir.
Fenitoin veya fenobarbital gibi enzim indükleyicilerin uygulanması metabolizmanın artmasına ve dolayısıyla serum kalsitriol düzeylerinin düşmesine neden olabilir. Bu nedenle, bu ilaçlar birlikte verilirse yüksek dozlarda kalsitriol gerekebilir.
Kolestiramin ve sevelamer dahil safra asitlerini tutan maddeler, yağda çözünen vitaminlerin bağırsak emilimini azaltabilir ve böylece kalsitriolün bağırsak emilimini değiştirebilir.
04.6 Hamilelik ve emzirme
Gebelik
Supravalvüler aort stenozu, hamile tavşanlara neredeyse ölümcül dozlarda D vitamini uygulandığında tavşan fetüslerinde meydana geldi. D vitamininin insanlarda çok yüksek dozlarda bile teratojenik olduğuna dair bir kanıt yoktur DIFIX hamilelikte ancak yararları fetüs için potansiyel riskten ağır basıyorsa kullanılmalıdır.
Besleme zamanı
Eksojen kalsitriolün anne sütüne geçtiği varsayılabilir. Annede hiperkalsemi olasılığı ve bebeklerde DIFIX'in advers reaksiyonları göz önüne alındığında, anne ve bebeğin serum kalsiyum düzeylerinin izlenmesi şartıyla anneler DIFIX alırken emzirebilir.
04.7 Araç ve makine kullanma yeteneği üzerindeki etkiler
Bildirilen advers olayların farmakodinamik profiline dayanarak, bu ürünün güvenli olduğu veya bu faaliyetler üzerindeki olumsuz etkisinin olası olmadığı varsayılmaktadır.
04.8 İstenmeyen etkiler
Klinik çalışmalar
Aşağıda listelenen advers reaksiyonlar, klinik denemeler sırasında ve pazarlama sonrası aşamada kalsitriol ile olan deneyimi yansıtmaktadır.
Hiperkalsemi en sık bildirilen advers reaksiyondur.
Tablo 1'de listelenen ADR'ler, sistem organ sınıfı ve sıklığına göre kategorize edilir ve aşağıdaki kural kullanılarak tanımlanır: Çok yaygın (≥1 / 10); yaygın (≥1 / 100 y
Tablo 1: Difix® (kalsitriol) ile tedavi edilen hastalarda bulunan ADR'lerin özeti
Kalsitriol D vitamini aktivitesini uyguladığından, çok fazla D vitamini alındığında görülenlere benzer yan etkiler ortaya çıkabilir, örn. hiperkalsemik sendrom veya kalsiyum intoksikasyonu (hiperkalseminin şiddetine ve süresine bağlı olarak) (bkz. bölüm 4.2 Pozoloji ve uygulama yöntemi). ve bölüm 4.4 Özel kullanım uyarıları ve önlemleri Ara sıra görülen akut semptomlar iştah azalması, baş ağrısı, bulantı, kusma, ağız kuruluğu, karın ağrısı veya üst karın ağrısı ve kabızlık, kemik ve kas ağrısını içerir.
Kalsitriolün kısa biyolojik yarı ömrü nedeniyle, farmakokinetik çalışmalar, yüksek serum kalsiyum düzeylerinin tedaviyi bıraktıktan sonraki birkaç gün içinde normale döndüğünü, yani D3 vitamini preparatları ile yapılan tedavilere göre çok daha hızlı olduğunu göstermiştir.
Kronik etkiler arasında kas zayıflığı, kilo kaybı, duyu bozuklukları, ateş, susuzluk, polidipsi, poliüri, dehidratasyon, apati, büyüme geriliği, idrar yolu enfeksiyonları sayılabilir.
> 6mg / 100ml veya 1.9mmol / L'lik hiperkalsemi ve hiperfosfatemi ile eşzamanlı olarak kalsinozis oluşabilir; bu fenomen radyografik olarak görülebilir.
Yatkınlığı olan kişilerde deri döküntüsü, eritem, kaşıntı ve ürtiker gibi aşırı duyarlılık reaksiyonları ortaya çıkabilir.
Laboratuvar Anomalileri
Normal böbrek fonksiyonu olan hastalarda, kronik hiperkalsemi, kan kreatininde bir artış ile ilişkili olabilir.
Pazarlama sonrası
Tüm endikasyonlar için 15 yıllık bir süre boyunca izlenen DIFIX'in klinik kullanımında bildirilen yan etkilerin sayısı çok düşüktür ve hiperkalsemi dahil herhangi bir tek etkinin insidans oranı %0,001 veya daha azdır.
Şüpheli advers reaksiyonların raporlanması
İlacın ruhsatlandırılmasından sonra meydana gelen şüpheli advers reaksiyonların raporlanması, tıbbi ürünün fayda/risk oranının sürekli olarak izlenmesine imkan verdiği için önemlidir.Sağlık profesyonellerinden, şüphelenilen advers reaksiyonları İtalyan İlaç Kurumu aracılığıyla bildirmeleri istenir, web sitesi web http://www.agenziafarmaco.gov.it/it/responsabili.
04.9 Doz aşımı
Asemptomatik hiperkalsemi tedavisi: (Bkz. bölüm 4.2 Pozoloji ve uygulama yöntemi).
Difix doz aşımı hiperkalsemiye ve bazı durumlarda hiperkalsiüriye neden olabileceğinden, doz ayarlama aşamasında kalsiyum en az haftada iki kez verilmelidir. Optimal günlük doz belirlendikten sonra, aylık kan kalsiyum kontrolü yeterlidir.
Kalsitriol, D vitamininin bir türevi olduğundan, doz aşımı belirtileri D vitamini ile aynıdır. Yüksek dozda kalsiyum ve fosfatın DIFIX ile birlikte alınması benzer belirtilere neden olabilir. fosfatemi (Ca XP) 70 mg2/dl2'yi geçmemelidir Diyaliz hastasında yüksek düzeyde kalsiyum hiperkalsemi gelişimine katkıda bulunabilir.
D vitamini zehirlenmesinin akut belirtileri: anoreksi, baş ağrısı, kusma, kabızlık.
Kronik semptomlar: distrofi (zayıflık, kilo kaybı), duyusal bozukluklar, susuzluk, poliüri, dehidratasyon, apati, bodur büyüme ve idrar yolu enfeksiyonlarının eşlik ettiği olası ateşli durumlar.
Hiperkalsemi renal korteks, miyokard, akciğerler ve pankreasta metastatik kalsifikasyona yol açabilir.
Kazara aşırı dozun tedavisinde aşağıdaki ihtiyati tedbirler dikkate alınmalıdır: daha fazla emilimi önlemek için hemen gastrik lavaj veya kusma indüksiyonu.
Fekal atılımı kolaylaştırmak için sıvı parafin uygulanabilir.Serum kalsiyumunun tekrarlanan ölçümleri tavsiye edilir.Yüksek serum kalsiyum seviyeleri devam ederse, fosfatlar ve kortikosteroidler uygulanabilir ve yeterli diürez elde etmek için önlemler alınabilir.
Yüksek seviyelere (> 3.2 mmol / L) kadar hiperkalsemi, özellikle kandaki fosfat seviyeleri normalse veya böbrek fonksiyon bozukluğu nedeniyle yükselmişse, böbrek yetmezliğine yol açabilir.
Herhangi bir D vitamini formunun aşırı dozu ciddi belirtilere bile neden olur.
Aşırı dozda D vitamini veya metabolitlerinin neden olduğu hiperkalsemi de acil tedavi gerektirebilir.
Olası kalsifikasyonların anatomik bölgelerinin radyografik muayenesi erken tanı için faydalı olabilir.
05.0 FARMAKOLOJİK ÖZELLİKLER
05.1 Farmakodinamik özellikler
Farmakoterapötik grup: Aktif D Vitamini.
ATC kodu: A11CC04
Kalsitriol, öncüsü 25-hidroksikolekasiferolden (25-HCC) böbrekte oluşan D3 vitamininin ana aktif metabolitlerinden biridir.
DIFIX, kalsiyumun bağırsak emilimini arttırır ve kemik mineralizasyonunu düzenler Şiddetli böbrek yetmezliği olan hastalarda, özellikle bir süredir periyodik hemodiyaliz uygulananlarda, endojen kalsitriol oluşumu giderek azalır ve hatta tamamen durabilir: bu eksiklik birincil bir rol oynar. Renal osteodistrofi başlangıcında rol oynar.
Renal osteodistrofi olan hastalarda, DIFIX'in oral uygulaması.
- kalsiyumun bağırsak emilimini normalleştirir;
- hipokalsemiyi düzeltir;
- kemik ve kas ağrılarını giderir.
Yönetim ayrıca şunları da destekler:
- alkalin fosfatazın serum seviyelerinin normalleştirilmesi veya azaltılması;
- paratiroid hormonu serum seviyelerinin normalleştirilmesi veya azaltılması.
Hem idiyopatik hem de cerrahi hipoparatiroidizmden mustarip hastalarda DIFIX, paratiroid hormon eksikliğine bağlı hipokalsemiyi düzeltir.
Psödohipoparatiroidizmde normal bağırsak kalsiyum emilimini yeniden oluşturmaya, hipokalsemiyi düzeltmeye ve dolaşımdaki paratiroid hormon düzeylerini düşürmeye izin verir.
D vitaminine dirençli hipofosfatemik raşitizmde DIFIX uygulaması klinik tablonun iyileşmesine ve dolaşımdaki fosfatların normalleşmesine yol açar.
Ailede D vitaminine bağlı raşitizmde DIFIX, kemik lezyonlarının remisyonunu ve kalsemik ve fosfat değerlerinin normalleşmesini ve bağırsaktan kalsiyum emilimini belirler.
Menopoz sonrası osteoporozdan mustarip hastalarda östrojen eksikliği, kalsitriolün endojen sentezinin azalmasına ve bunun sonucunda bağırsakta kalsiyum emilimi ve kemik mineralizasyon süreçlerinde bir azalmaya yol açar.
DIFIX uygulaması bağırsak kalsiyum emiliminde önemli bir artış belirler, bu şekilde bu hastalarda negatif olan kalsiyum dengesi pozitife döner.
05.2 Farmakokinetik özellikler
Hem trityum etiketli hem de etiketsiz kalsitriol ile sağlıklı deneklerde yapılan çalışmalar, ilaç emiliminin oral uygulamadan sonra hızla gerçekleştiğini ve 3-6 saat içinde maksimum seviyelere ulaştığını göstermektedir.
Hızlı emilim, uygulamadan yedi saat sonra doğrulanabilen idrardaki kalsiyumdaki hızlı artış ile doğrulanır.
"Günde iki kez uygulanan 0.5 ve 1.0 mcg'lik dozlarla idrarda artan kalsiyum atılımında doza bağlı bir biyolojik yanıt kanıtlanmıştır. Günde iki kez 0.5 mcg'lik dozlarla elde edilen kararlı durum değerleri, başlangıç seviyelerine düşerler. İlacın kesilmesinin ardından, yarılanma ömrü yaklaşık üç buçuk saattir.
05.3 Klinik öncesi güvenlik verileri
Kalsitriolün akut toksisitesi farelerde ve sıçanlarda değerlendirildi.
Oral uygulamadan sonra farelerde LD50, 2 mg/kg'a eşittir.
Sıçanda > 5 mg/kg'dır.
Kalsitriolün kronik toksisitesi sıçanlarda ve köpeklerde değerlendirilmiştir.
Bileşik, 26 hafta boyunca 0.02, 0.08 ve 0.30 mcg / kg / gün dozlarında oral olarak üç grup sıçan ve köpek uygulandı.Orta ve yüksek dozlar alan sıçan gruplarında vücutta bir azalma oldu. ağırlık, gıda alımında azalma, serum kalsiyumunda artış; bu değişiklikler daha düşük doz alan grupta yoktu veya daha az belirgindi.
Yüksek ve orta dozlarda verilen köpeklerde belirgin anoreksi, şiddetli kilo kaybı, fiziksel durumda bozulma, kalsiyum artışı, metastatik yumuşak doku kalsifikasyonu ve kemik değişiklikleri görülmüştür.
0.02 mcg/kg/gün alan gruptaki köpeklerde bu bulgular hafifledi.
06.0 FARMASÖTİK BİLGİLER
06.1 Yardımcı maddeler
0.25 mcg kapsüller: butilhidroksianisol, butilhidroksitoluen, orta zincirli trigliseritler, jelatin, gliserol, %85 sorbitol çözeltisi, sorbitanlar ve mannitol, etil-p-oksibenzoat sodyum tuzu (E 215), propil-p-oksibenzoat tuzu sodyum (E 217), titanyum dioksit (E 171).
0,50 mcg kapsüller: butilhidroksianisol, butilhidroksitoluen, orta zincirli trigliseritler, jelatin, gliserol, %85 sorbitol çözeltisi, sorbitanlar ve mannitol, etil-p-oksibenzoat sodyum tuzu (E 215), propil-p-oksibenzoat tuzu sodyum (E 217), titanyum dioksit (E 171), kantaksantin %10 (E 161).
06.2 Uyumsuzluk
Bugüne kadar belirli bir uyumsuzluk bilinmemektedir.
06.3 Geçerlilik süresi
3 yıl
06.4 Depolama için özel önlemler
30 ° C'nin altındaki bir sıcaklıkta saklayın.
06.5 İç ambalajın yapısı ve paketin içeriği
İç ambalaj: PA / Al / PVC-Al bağlantılı blister ambalajlar.
Dış ambalaj: baskılı karton kutu.
DIFIX 0.25 mcg yumuşak kapsüller
30 kapsüllük kutu
DIFIX 0,50 mcg yumuşak kapsüller
30 kapsüllük kutu
06.6 Kullanım ve kullanım talimatları
Özel talimat yok
07.0 PAZARLAMA YETKİ SAHİBİ
PROMEDICA S.r.l. - Via Palermo 26 / A - 43100 Parma.
08.0 PAZARLAMA YETKİ NUMARASI
Difix 0.25 mcg yumuşak kapsül - 30 kapsül
N ° 027231012
Difix 0.50 mcg yumuşak kapsül - 30 kapsül
N° 027231036
09.0 İLK İZİN VEYA İZİNİN YENİLENMESİ TARİHİ
15/04/1996
10.0 METİN REVİZYON TARİHİ
Ekim 2013





















-cos-cause-sintomi-e-rimedi.jpg)


