Aktif maddeler: Hidrojen peroksit
KRİSTAZİT - %1 krem
Kristasit neden kullanılır? Bu ne için?
farmakoterapötik grup
Dezenfektan.
Tedavi endikasyonları
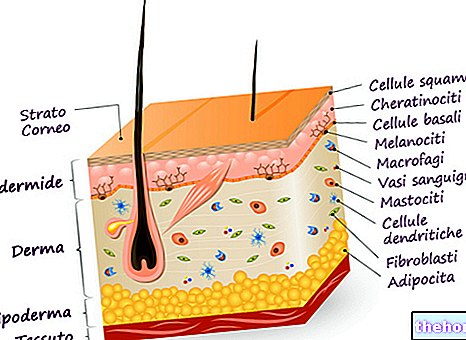
CRYSTACIDE CREAM, hidrojen peroksite duyarlı organizmaların neden olduğu birincil ve ikincil yüzeysel cilt enfeksiyonlarının tedavisinde topikal uygulama için formüle edilmiştir.
Kontrendikasyonlar Crystacide kullanılmamalıdır
Ürünün bir veya daha fazla yardımcı maddesine karşı bilinen aşırı duyarlılık.
Kullanım Önlemleri Crystacide kullanmadan önce bilmeniz gerekenler
Gözlerle temasından kaçının. Ürün göze temas ederse hemen bol soğuk su ile yıkayınız. Hidrojen peroksit dokuları beyazlatabilir. Salisilik asit hafif bir tahriş edicidir ve dermatite neden olabilir.
Crystacide Cream ayrıca cilt tahrişine neden olabilen propilen glikol içerir.
Etkileşimler Hangi ilaçlar veya yiyecekler Crystacide'in etkisini değiştirebilir?
CRYSTACIDE CREMA, iyot, permanganatlar ve diğer daha güçlü oksitleyici ajanlarla uyumsuzdur.
Uyarılar Şunları bilmek önemlidir:
Hamilelik ve emzirme: Tıbbi gözetim altında kullanın.
Doz, Uygulama Yöntemi ve Zamanı Crystacide nasıl kullanılır: Pozoloji
CRYSACIDE CREMA, titanyum dioksit ile renklendirilmiş ve polipropilen kapaklı polietilen tüplerde bulunur. Her bir tüp 25 gr, 40 gr, 10 gr, 5 gr baskılı karton ambalajlarda bulunmaktadır.
Yetişkinlerde, yaşlılarda ve çocuklarda kullanım
CRYSTASİD KREM, cildin enfekte olan kısmına günde 2-3 kez uygulanır. Yaranın üzerinde, bölgeyi suyla yıkayarak çıkarılabilen kuru bir film görünebilir.
Tedavi süresi
Tedavi süresi 3 haftayı geçmemelidir.
Yan Etkiler Crystacide'in yan etkileri nelerdir?
CRYSACIDE CREAM genellikle iyi tolere edilir ve herhangi bir ciddi yan etki ile ilişkili değildir. Ancak uygulamadan sonra kısa bir süre hafif bir yanma hissi olabilir.Uzun süreli cilt tahrişi veya kullanma talimatında belirtilmese de diğer istenmeyen etkiler durumunda hasta doktoruna veya eczacısına haber vererek durumu sorması istenir. ilacın uygulanması durdurulmalıdır.
Yan etkilerin raporlanması
Herhangi bir yan etki yaşarsanız, doktorunuzla veya eczacınızla konuşun.Bu kullanma talimatında listelenmeyen olası yan etkiler de buna dahildir. Yan etkiler doğrudan www.agenziafarmaco.it/it/responsabili adresindeki ulusal raporlama sistemi aracılığıyla da bildirilebilir.Yan etkileri bildirerek bu ilacın güvenliği hakkında daha fazla bilgi sağlamaya yardımcı olabilirsiniz.
Son Kullanma ve Saklama
Paket üzerinde belirtilen son kullanma tarihinden sonra ilacı kullanmayınız.
Diğer bilgiler
Kompozisyon
1 gr krem şunları içerir:
- Aktif madde 10mg hidrojen peroksit.
- Yardımcı maddeler Gliseril monolaurat, Gliseril monomiristat, makrogol stearat 5000, Propilen glikol, Sitrik asit susuz, Sodyum hidroksit, Sülfürik asit, Sodyum oksalat, Salisilik asit, Disodyum edetat, Sodyum pirofosfat, Sodyum stanat, Arıtılmış su.
Farmasötik form
Krem.
Kaynak Paket Broşürü: AIFA (İtalyan İlaç Ajansı). Ocak 2016'da yayınlanan içerik. Mevcut bilgiler güncel olmayabilir.
En güncel sürüme erişmek için AIFA (İtalyan İlaç Ajansı) web sitesine erişmeniz önerilir. Sorumluluk reddi ve faydalı bilgiler.
Crystacide hakkında daha fazla bilgi "Özellikler Özeti" sekmesinde bulunabilir. 01.0 TIBBİ ÜRÜNÜN ADI 02.0 KALİTATİF VE KANTİTATİF BİLEŞİM 03.0 FARMASÖTİK FORM 04.0 KLİNİK ÖZELLİKLER 04.1 Terapötik endikasyonlar 04.2 Pozoloji ve uygulama yöntemi 04.3 Kontrendikasyonlar 04.4 Özel kullanım uyarıları ve uygun önlemler 04.5 Diğer tıbbi ürünlerle etkileşimler ve diğer formlarla etkileşimler0 ve laktasyon 04.7 Araç ve makine kullanma yeteneği üzerindeki etkiler 04.8 İstenmeyen etkiler 04.9 Doz aşımı05.0 FARMAKOLOJİK ÖZELLİKLER05.1 Farmakodinamik özellikler05.2 Farmakokinetik özellikler05.3 Klinik öncesi güvenlilik verileri06.0 BİLGİ FARMASÖTİKLER 06.1 Yardımcı maddeler 06.2 Geçimsizlikler 06.3 Raf ömrü 06.4 Özel önlemler depolama için 06.5 Ambalajın yapısı ve ambalajın içeriği 06.6 Kullanım ve elleçleme talimatları 07.0 PAZARLAMA YETKİ SAHİBİ08 .0 PAZARLAMA İZNİ NUMARASI 09.0 İLK TARİH İZİNİN İZNLENMESİ VEYA YENİLENMESİ 10.0 METİN REVİZYON TARİHİ 11.0 RADYO İLAÇLAR İÇİN, DAHİLİ RADYASYON DOZİMETRİ HAKKINDA TAM VERİLER 12.0 RADYO İLAÇLAR İÇİN, ESANDEPORANEA HAZIRLANMASI HAKKINDA AYRINTILI TALİMATLAR
01.0 TIBBİ ÜRÜNÜN ADI
KRİSTAZİT KREM TÜMÜ "1%
02.0 KALİTATİF VE KANTİTATİF BİLEŞİM
Aktif prensip
%1.0 (a/a) hidrojen peroksit.
1 gram krem, %1 konsantrasyonda 10 mg hidrojen peroksit içerir.
03.0 FARMASÖTİK FORM
Krem.
04.0 KLİNİK BİLGİLER
04.1 Terapötik endikasyonlar
Crystacide krem, hidrojen peroksite duyarlı organizmaların neden olduğu birincil ve ikincil yüzeysel cilt enfeksiyonlarının tedavisinde topikal uygulama için formüle edilmiştir.
04.2 Pozoloji ve uygulama yöntemi
Yetişkinler, yaşlılar ve çocuklar : Crystacide krem günde 2-3 defa cildin enfeksiyonlu bölgesine sürülür. Tedavi süresi 3 haftayı geçmemelidir. Yaranın üzerinde, bölgeyi suyla yıkayarak çıkarılabilen kuru bir film görünebilir.
04.3 Kontrendikasyonlar
Etkin maddeye veya yardımcı maddelerden herhangi birine karşı aşırı duyarlılık.
04.4 Özel uyarılar ve uygun kullanım önlemleri
Gözlerle temasından kaçının. Crystacide krem, büyük veya derin yaralarda veya sağlıklı ciltlerde kullanılmamalıdır. Hidrojen peroksit dokuları beyazlatabilir.
Salisilik asit hafif bir tahriş edicidir ve dermatite neden olabilir.
Crystacide Cream ayrıca cilt tahrişine neden olabilen propilen glikol içerir.
04.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim biçimleri
Crystacide krem, iyot, permanganatlar ve diğer daha güçlü oksitleyici ajanlarla uyumsuzdur.
04.6 Hamilelik ve emzirme
Tıbbi gözetim altında kullanılacak
04.7 Araç ve makine kullanma yeteneği üzerindeki etkiler
Uygulanamaz.
04.8 İstenmeyen etkiler
Uygulamadan sonra kısa bir süre hafif bir yanma hissi hissedilebilir.
Şüpheli advers reaksiyonların raporlanması
İlacın ruhsatlandırılmasından sonra meydana gelen şüpheli advers reaksiyonların raporlanması, tıbbi ürünün fayda/risk dengesinin sürekli olarak izlenmesine imkan verdiği için önemlidir. Sağlık profesyonellerinden şüpheli advers reaksiyonları ulusal raporlama sistemi aracılığıyla bildirmeleri istenir. "Sokak adresi www.aifa.gov.it/responsabili.
04.9 Doz aşımı
Uygulanamaz
05.0 FARMAKOLOJİK ÖZELLİKLER
05.1 Farmakodinamik özellikler
ATC kodu: D08A.
Antiseptikler ve dezenfektanlar.
Hidrojen peroksit, çoğu patojenik mikroorganizmaya karşı etkili, iyi bilinen bir antiseptik maddedir.
In vitro farmakolojik çalışmalar, hidrojen peroksitin çok çeşitli mikroorganizmalara karşı etkili olduğunu ve Gram pozitif ve Gram negatif bakterilere karşı etkili güçlü bir antibakteriyel olduğunu göstermiştir.
In vitro çalışmalar, Crystacide %1 kreminin bakterisit aktivitesinin, %1 sulu hidrojen peroksit çözeltisi ile elde edilenlerle aynı etkilere sahip olduğunu ve kremin daha uzun bir etki süresine sahip olduğunu göstermiştir.
Hidrojen peroksite direnç geliştiren bilinen patojenik bakteri veya mantar yoktur.
05.2 Farmakokinetik özellikler
Oral uygulamadan sonra hidrojen peroksitin absorpsiyon, dağılım ve eliminasyon hızına ilişkin veriler sınırlıdır. Stabilize edici bir maddenin yokluğunda, hidrojen peroksit yavaş yavaş oksijen ve suya ayrışır. Ayrışma, endojen katalaz veya peroksidaz enziminin varlığında hızlıdır.
05.3 Klinik öncesi güvenlik verileri
KÜB'ün diğer bölümlerinde zaten bulunanlara eklemek için reçeteyi uygulayanlar için ilgili klinik öncesi veri yoktur.
06.0 FARMASÖTİK BİLGİLER
06.1 Yardımcı maddeler
gliseril monolaurat
gliseril monomiristat
Makrogol stearat 5000
propilen glikol
susuz sitrik asit
Sodyum hidroksit
Sülfürik asit, 1M
sodyum oksalat
Salisilik asit
disodyum edetat
sodyum pirofosfat
sodyum stannat
Arıtılmış su
06.2 Uyumsuzluk
İyot, permanganatlar ve diğer daha güçlü oksitleyici maddeler.
06.3 Geçerlilik süresi
2 yıl.
Konteyneri ilk açtıktan sonra: 28 gün.
06.4 Depolama için özel önlemler
25°C'nin altında, kuru bir yerde saklayınız.
06.5 İç ambalajın yapısı ve paketin içeriği
Crystacide krem, titanyum dioksit ile renklendirilmiş ve bir polipropilen kapak ile donatılmış polietilen tüplerde bulunur. Her bir tüp, 5 gr, 10 gr, 25 gr ve 40 gr formatlarında baskılı karton ambalaj içerisinde yer almaktadır.
06.6 Kullanım ve kullanım talimatları
Uygulanamaz.
07.0 PAZARLAMA YETKİ SAHİBİ
Giuliani S.p.a.
Via Palagi, 2
20129 Milano
08.0 PAZARLAMA YETKİ NUMARASI
5g tüp-AIC: 034220018
10g tüp-AIC: 034220020
25g tüp-AIC: 034220032
40g tüp-AIC: 034220044
09.0 İLK İZİN VEYA İZİNİN YENİLENMESİ TARİHİ
1 Nisan 1999/17 Ocak 2006
10.0 METİN REVİZYON TARİHİ
20 Haziran 2016