Aktif maddeler: Triptorelin
DECAPEPTYL 0.1 mg / ml Enjeksiyonluk çözelti için toz ve çözücü
Paket boyutları için Decapeptyl paket ekleri mevcuttur:- DECAPEPTYL 0.1 mg / ml Enjeksiyonluk çözelti için toz ve çözücü
- DECAPEPTYL 3,75 mg / 2 ml enjeksiyonluk uzun süreli salımlı süspansiyon için toz ve çözücü
- Decapeptyl 11.25 mg / 2 ml enjeksiyonluk uzun süreli salımlı süspansiyon için toz ve çözücü
Decapeptyl neden kullanılır? Bu ne için?
FARMAKOTERAPÖTİK KATEGORİ
Endokrin tedavisi, hormon salgılayan gonadotropinlerin analogu
TEDAVİ ENDİKASYONLARI
Ovulasyon indüksiyon protokollerinde, embriyo transferi (F.I.V.E.T.) ardından embriyo transferi (F.I.V.E.T.) ve yardımcı üreme için diğer teknikler bağlamında, yumurtlama indüksiyon protokollerinde gonadotropinlerle birlikte kadınlarda kısırlığın tedavisi.
Kontrendikasyonlar Decapeptyl kullanılmamalıdır
GnRH'ye, analoglarına veya tıbbi ürünün yardımcı maddelerinden herhangi birine karşı aşırı duyarlılık (bkz. 4.8). Hamilelik ve emzirme.
Kullanım Önlemleri Decapeptyl'i almadan önce bilmeniz gerekenler
GnRH agonistlerinin kullanımı kemik mineral yoğunluğunda azalmaya neden olabilir.
Osteoporoz için ek risk faktörlerine sahip hastalarda (örn.kronik alkol kötüye kullanımı, sigara içme, antikonvülzanlar veya kotikoidler gibi kemik mineral yoğunluğunu azaltan ilaçlarla uzun süreli tedavi, ailede osteoporoz öyküsü, yetersiz beslenme)
Triptorelin reçete edilmeden önce hastanın hamile olmadığının doğrulanması gerekir.
Nadiren, GnRH agonistleri ile tedavi, önceden bilinmeyen bir gonadotropik hücreli hipofiz adenomunun varlığını ortaya çıkarabilir. Bu hastalar ani baş ağrısı, kusma, görme bozukluğu ve oftalmopleji ile karakterize hipofiz apopleksisi ile başvurabilirler.
Decapeptyl alan hastalarda şiddetli olabilen depresyon da dahil olmak üzere duygudurum değişiklikleri rapor edilmiştir.Dekapeptyl alıyorsanız ve depresif ruh hali geliştirirseniz, lütfen doktorunuzu bilgilendirin.Hastalar tedavi sırasında yakından izlenmelidir.Bilinen depresyonu olan hastalar.
Androjen yoksunluğu tedavisi QT aralığını uzatabilir.
QT aralığı uzaması öyküsü olan veya QT aralığı uzaması için risk faktörleri olan hastalarda ve eşzamanlı olarak QT aralığını uzatabilen ilaçlar alan hastalarda (bkz. Torsade de Pointes olasılığı da dahil.
Kadınlar
Kemik mineral yoğunluğunda azalma
GnRH agonistlerinin kullanımının, 6 aylık bir tedavi süresi boyunca, ortalama olarak, kemik mineral yoğunluğunda ayda %1'lik bir azalmaya neden olması muhtemeldir. Kemik mineral yoğunluğundaki her %10'luk azalma, kırık riskini 2 ila 3 kat artırır.
Halihazırda mevcut veriler, çoğu kadında kemik yoğunluğunun restorasyonunun tedavinin kesilmesinden sonra gerçekleştiğini göstermektedir.
Doğrulanmış osteoporozu veya osteoporoz için risk faktörleri olan hastalar (örn. kronik alkol kötüye kullanımı, sigara içenler, antikonvülzanlar veya kortikoidler gibi kemik mineral yoğunluğunu azaltan ilaçlarla uzun süreli tedaviler, ailede osteoporoz öyküsü, yetersiz beslenme, örn. anoreksiya nervoza) Bu hastalarda kemik mineral yoğunluğundaki azalmanın daha zararlı olması muhtemel olduğundan, triptorelin tedavisi bireysel olarak düşünülmeli ve çok dikkatli bir değerlendirmeden sonra ancak tedavinin yararları risklerinden ağır basıyorsa başlatılmalıdır. Kemik mineral yoğunluğu kaybını önlediği düşünülür.
Kadın kısırlığı
0.1 mg triptorelin reçete etmeden önce, hastanın hamile olmadığının doğrulanması gerekir.
GnRH analoglarının ve gonadotropinlerin kullanımıyla indüklenen foliküler stimülasyon, özellikle Polikistik Over Sendromu durumunda, yatkın hastaların azınlıkta önemli ölçüde arttırılabilir.
Decapeptyl - gonadotropin kombinasyonuna yumurtalık yanıtı, aynı dozda bile bir hastadan diğerine ve bazı durumlarda aynı hastada bir döngüden diğerine değişebilir.
Ovulasyon düzenli klinik ve biyolojik kontrollerle yakından izlenmelidir: ultrason muayeneleri ve plazma östrojenlerinin değerlendirilmesi
Diğer GnRH analoglarında olduğu gibi, gonadotropinlerle kombinasyon halinde triptorelin kullanımıyla ilişkili ovaryan hiperstimülasyon sendromu (OHSS) raporları olmuştur.
Predispoze hastalarda meydana gelebilecek over hiper-yanıtı durumunda veya overin polikistik hastalığı durumunda, gonadotropin uygulamasının durdurulması tavsiye edilirken, Decapeptyl 0.1 mg uygulamasına birkaç gün devam edilir. olası bir spontan LH dalgalanması.
Etkileşimler Hangi ilaçlar veya yiyecekler Decapeptyl'in etkisini değiştirebilir?
Triptorelin, gonadotropinlerin hipofiz salgısını etkileyen diğer ilaçlarla birlikte uygulandığında dikkatli olunmalı ve hastanın hormonal durumunun izlenmesi önerilir.
Androjen yoksunluğu tedavisi QT aralığını uzatabileceğinden, Decapeptyl 0.1 mg'ın QT aralığını uzattığı bilinen tıbbi ürünlerle veya antiaritmik tıbbi ürünler gibi Torsades de Pointes'i indükleyebilen tıbbi ürünlerle birlikte kullanımı dikkatle değerlendirilmelidir. , disopiramid) veya sınıf III (örn. amiodaron, sotalol, dofetilid, ibutilid), metadon, moksifloksasin, antipsikotikler vb. (Kullanım önlemleri bölümüne bakınız).
Uyarılar Şunları bilmek önemlidir:
Hamilelik ve emzirme
Gebelik
GnRH agonistlerinin birlikte kullanımı teorik bir düşük veya fetal anormallik riski ile ilişkili olduğundan, triptorelin hamilelik sırasında kullanılmamalıdır. adet döngüsü dönene kadar tedavi.
Triptorelin infertilite tedavisi için kullanılmadan önce gebelik ekarte edilmelidir.Bu durumda triptorelin kullanıldığında, triptorelin ile oosit gelişimindeki sonraki anormallikler arasında nedensel bir ilişki olduğunu gösteren klinik kanıt yoktur. gebelik.
Besleme zamanı
Triptorelin emzirme döneminde kullanılmamalıdır.
Araç ve makine kullanma
Triptorelin farmakolojik profili göz önüne alındığında, triptorelin hastanın araç veya makine kullanma yeteneği üzerinde muhtemelen hiçbir etkisi yoktur veya ihmal edilebilir düzeydedir.
Sportif faaliyetlerde bulunanlar için
İlacın terapötik gereklilik olmaksızın kullanılması doping teşkil eder ve her durumda pozitif anti-doping testleri belirleyebilir.
Dozaj ve kullanım yöntemi Decapeptyl nasıl kullanılır: Dozaj
Tıbbi reçeteye kesinlikle uyun.
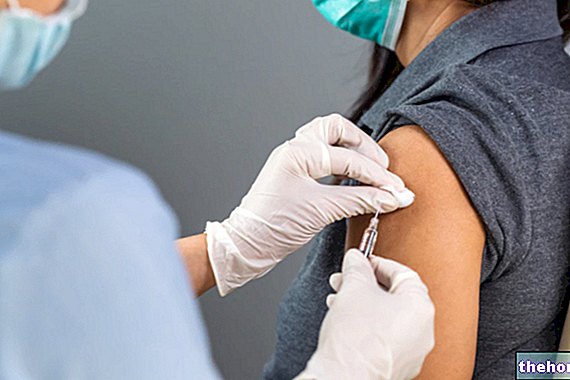
Kısa protokol: Adet döngüsünün ikinci gününden (yumurtalık stimülasyonunun başlangıcına denk gelen) başlayarak hCG uygulamasından önceki güne kadar günde 0.1 mg 1 flakon Decapeptyl subkutan olarak, ortalama 10-12 gün süreyle uygulayın.
Uzun protokol: Adet döngüsünün ikinci gününden başlayarak günde 1 flakon Decapeptyl 0.1 mg deri altından uygulanır. Hipofiz duyarsızlaşması sağlandıktan sonra (genellikle tedavinin 15. gününde plazma östrojen konsantrasyonu 50 pg/ml'nin altında), hCG uygulamasından önceki güne kadar 0.1 mg Decapeptyl ile eş zamanlı olarak gonadotropin stimülasyonuna başlayın.
İlaç, hazırlıksız hazırlıktan sonra deri altından uygulanır.
Şırınga ile flakonun içeriğini çekin ve flakondaki tüm sıvıyı flakona aktarın. Homojen bir çözelti sağlamak için flakonu ters çevirmeden hafifçe sallayın. Derhal enjeksiyona geçin.
N.B.: Enjeksiyonun kullanım talimatlarına tam olarak uyularak yapılması önemlidir.
Doz aşımı Çok fazla Decapeptyl aldıysanız ne yapmalısınız?
Doz aşımının bir sonucu olarak herhangi bir advers reaksiyon bildirilmemiştir. Yanlışlıkla tavsiye edilenden daha yüksek doz alınması durumunda vakit kaybetmeden doktorunuza başvurunuz.
Yan Etkiler Decapeptyl'in yan etkileri nelerdir?
GnRH analogları alan hastalarda artmış lenfosit sayıları bildirilmiştir.
Klinik çalışmalarda deneyim
Klinik çalışmalara katılan ve hızlı salimli formülasyon olan triptorelin ile tedavi edilen yetişkin popülasyonda, 3 ay boyunca günlük tedavi edilen prostat kanserli 127 erkek ve in vitro fertilizasyon protokolleri uygulanan yaklaşık 1.000 kadın yer aldı. Erkeklerde ve kadınlarda 3.75 mg ve 11.25 mg triptorelin formülasyonları ile gerçekleştirilen klinik deneyler sırasında kazanılan ayrıntılı güvenlik deneyimi de dahil edilmiştir.
Klinik çalışmalardan elde edilen güvenlik deneyiminin genel analizi, hipogonadotropik hipogonadizm veya bazen ilk hipofiz-gonadal stimülasyonun bir sonucu olarak ilaç sınıfına bağlı advers reaksiyonları içermiştir.
Advers reaksiyonların sıklığı şu şekilde sınıflandırılmıştır: çok yaygın (≥1/10) - Yaygın (≥1/100-
Yetişkinlerde genel tolere edilebilirlik
Çok yaygın: Genellikle tedavinin kesilmesini gerektirmeyen hafif ila şiddetli sıcak basmaları Yaygın: psikiyatrik bozukluklar (ruh hali değişimleri, depresyon) *
Yaygın olmayan: psikiyatrik bozukluklar (ruh hali değişiklikleri, depresyon) **
Bilinmeyen: QT aralığı uzaması (Kullanım önlemleri ve Etkileşimler bölümlerine bakın)
* Uzun süreli kullanım. Bu frekans, tüm GnRH agonistlerinde ortak olan sınıf etkisinin frekansına dayanmaktadır.
** Kısa süreli kullanım. Bu frekans, tüm GnRH agonistlerinde ortak olan sınıf etkisinin frekansına dayanmaktadır.
Kadınlarda genel tolere edilebilirlik
Tedavinin başlangıcında çok yaygın: Kısırlık tedavisinde triptorelin gonadotropinlerle birlikte kullanıldığında over hiperstimülasyon sendromu verebilir.Ovaryan hipertrofi, dispne, pelvik ve/veya karın ağrısı oluşabilir.
Aylık ve üç aylık formülasyonlarda triptorelin tedavisinin başlangıcında çok yaygın: İlk enjeksiyonu takip eden ayda menoraji veya metroraji dahil genital kanamalar olabilir.
Aylık ve üç aylık formülasyonlarda triptorelin tedavisi sırasında çok yaygın: bu advers reaksiyonlar, uyku bozuklukları, baş ağrısı, duygudurum değişikliği, vulvo-vajinal kuruluk ve disparoni, libido azalması gibi hipofiz-yumurtalık bloğu ile ilgili bir dizi hipo-östrojenik olayı gösterir.
Aylık formülasyonda triptorelin tedavisi sırasında yaygın: göğüs ağrısı, kas spazmları, artralji, kilo alımı, mide bulantısı, karında rahatsızlık/ağrı, asteni. Uzun süreli kullanımda ruh hali değişiklikleri ve depresyon bildirilmiştir.
Yerel tolere edilebilirlik
Çok nadir: enjeksiyon bölgesinde ağrı, eritem ve iltihaplanma.
Pazarlama sonrası bilgiler
Pazarlama sonrası gözetim sırasında IVF tedavisi gören kadınlarda başka istenmeyen etkiler bildirilmiştir. İstenmeyen etkiler, sistemik organik kategorilere göre ve bildirilen etkilerin azalan sıklık sırasına göre sınıflandırılır:
Deri ve deri altı doku bozuklukları: kaşıntı, kurdeşen, döküntü, anjiyonörotik ödem dahil aşırı duyarlılık reaksiyonları ("Kontrendikasyonlar" bölümüne bakın)
Sinir sistemi bozuklukları: baş ağrısı
Göz bozuklukları: bulanık görme veya görme bozuklukları bölümleri.
Bu kullanma talimatında listelenmeyen olası yan etkiler de dahil olmak üzere herhangi bir yan etki yaşarsanız, doktorunuza veya eczacınıza danışınız. Yan etkiler ayrıca https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse adresindeki ulusal raporlama sistemi aracılığıyla da doğrudan bildirilebilir.Yan etkileri bildirerek bu ilacın güvenliği hakkında daha fazla bilgi sağlamaya yardımcı olabilirsiniz.
Son Kullanma ve Saklama
Son kullanma tarihi: paketin üzerinde belirtilen son kullanma tarihine bakın.
Uyarı: Paket üzerinde belirtilen son kullanma tarihinden sonra ilacı kullanmayınız.
Belirtilen son kullanma tarihi, doğru şekilde saklanmış, bozulmamış ambalajdaki ürüne karşılık gelir.
Özel saklama koşulları yok
Bu ilacı çocukların erişemeyeceği ve göremeyeceği bir yerde saklayın.
KOMPOZİSYON
Toz şişesi şunları içerir:
Aktif madde: Triptorelin 0.1 mg
Yardımcı maddeler: mannitol
Çözücü şişesi şunları içerir:
sodyum klorür, enjeksiyonluk su
FARMASÖTİK FORM VE İÇERİĞİ
Enjeksiyonluk çözelti için toz ve çözücü.
Deri altı kullanımı.
Paket 7 toz flakon, 1 ml'lik 7 solvent flakon içerir.
Kaynak Paket Broşürü: AIFA (İtalyan İlaç Ajansı). Ocak 2016'da yayınlanan içerik. Mevcut bilgiler güncel olmayabilir.
En güncel sürüme erişmek için AIFA (İtalyan İlaç Ajansı) web sitesine erişmeniz önerilir. Sorumluluk reddi ve faydalı bilgiler.
01.0 TIBBİ ÜRÜNÜN ADI
DECAPEPTYL 0.1 MG / ML TOZ VE ENJEKSİYON ÇÖZELTİ İÇİN ÇÖZÜCÜ
02.0 KALİTATİF VE KANTİTATİF BİLEŞİM
Her bir toz şişesi şunları içerir:
Aktif madde: Triptorelin 0.1 mg
Yardımcı maddeler için bkz. 6.1.
03.0 FARMASÖTİK FORM
Enjeksiyonluk çözelti için toz ve çözücü.
Deri altı kullanımı.
04.0 KLİNİK BİLGİLER
04.1 Terapötik endikasyonlar
Kadınlarda kısırlığın gonadotropinler (hMG, hCG, FSH) ile birlikte ovulasyon indüksiyon protokollerinde, tüp bebek ve ardından embriyo transferi (F.I.V.E.T.) bağlamında ve yardımcı üremeye yönelik diğer tekniklerde tedavisi.
04.2 Pozoloji ve uygulama yöntemi
Kısa protokol: Adet döngüsünün ikinci gününden (yumurtalık stimülasyonunun başlangıcına denk gelen) başlayarak, hCG uygulamasından önceki güne kadar günde 1 flakon Decapeptyl 0.1 mg deri altından, ortalama 10-12 gün süreyle uygulayın.
Uzun protokol: Adet döngüsünün ikinci gününden başlayarak günde 0,1 mg 1 flakon Decapeptyl subkutan olarak uygulayın. Hipofiz duyarsızlaşması sağlandıktan sonra (genellikle tedavinin 15. gününde plazma östrojen konsantrasyonu 50 pg/ml'nin altında), hCG uygulamasından önceki güne kadar 0.1 mg Decapeptyl ile eş zamanlı olarak gonadotropin stimülasyonuna başlayın.
İlaç, hazırlıksız hazırlıktan sonra deri altından uygulanır.
Şişenin içeriğini şırınga ile geri çekin ve sıvıyı flakondan flakona aktarın. Homojen bir çözelti sağlamak için flakonu ters çevirmeden hafifçe sallayın. Derhal enjeksiyona geçin.
Not: Enjeksiyonun kullanım talimatlarına harfiyen uyularak yapılması önemlidir.
04.3 Kontrendikasyonlar
GnRH'ye, analoglarına veya tıbbi ürünün yardımcı maddelerinden herhangi birine karşı aşırı duyarlılık (bkz. 4.8). Hamilelik ve emzirme.
04.4 Özel uyarılar ve uygun kullanım önlemleri
GnRH agonistlerinin kullanımı kemik mineral yoğunluğunda azalmaya neden olabilir.
Osteoporoz için ek risk faktörleri (örneğin kronik alkol kötüye kullanımı, sigara kullanımı, antikonvülzanlar veya kortikoidler gibi kemik mineral yoğunluğunu azaltan ilaçlarla uzun süreli tedavi, ailede osteoporoz öyküsü, yetersiz beslenme) olan hastalarda özel dikkat gösterilmelidir.
Triptorelin reçete edilmeden önce hastanın hamile olmadığının doğrulanması gerekir.
Nadiren, GnRH agonistleri ile tedavi, önceden bilinmeyen bir gonadotropik hücreli hipofiz adenomunun varlığını ortaya çıkarabilir. Bu hastalar ani baş ağrısı, kusma, görme bozukluğu ve oftalmopleji ile karakterize hipofiz apopleksisi ile başvurabilirler.
Depresyon da dahil olmak üzere duygudurum değişiklikleri bildirilmiştir Triptorelin gibi GnRH agonistleri ile tedavi gören hastalarda depresyon (şiddetli olabilir) insidansında artış vardır.
Semptomların ortaya çıkması durumunda hastalar bilgilendirilmeli ve uygun şekilde tedavi edilmelidir.
Bilinen depresyonu olan hastalar tedavi sırasında yakından izlenmelidir.
Kadınlar
Kemik mineral yoğunluğunda azalma
GnRH agonistlerinin kullanımının, 6 aylık bir tedavi süresi boyunca, ortalama olarak, kemik mineral yoğunluğunda ayda %1'lik bir azalmaya neden olması muhtemeldir. Kemik mineral yoğunluğundaki her %10'luk azalma, kırık riskini 2 ila 3 kat artırır.
Halihazırda mevcut veriler, çoğu kadında kemik yoğunluğunun restorasyonunun tedavinin kesilmesinden sonra gerçekleştiğini göstermektedir.
Doğrulanmış osteoporozu olan veya osteoporoz için risk faktörleri olan hastalar (örn. kronik alkol kötüye kullanımı, sigara içenler, antikonvülsanlar veya kortikoidler gibi kemik mineral yoğunluğunu azaltan ilaçlarla uzun süreli tedaviler, ailede osteoporoz öyküsü, yetersiz beslenme, örn. anoreksiya nervoza) Bu hastalarda azalmış kemik mineral yoğunluğunun daha zararlı olması muhtemel olduğundan, triptorelin tedavisi bireysel olarak düşünülmeli ve çok dikkatli bir değerlendirmeden sonra ancak tedavinin yararları risklerinden ağır basıyorsa başlatılmalıdır. kemik mineral yoğunluğu kaybı.
Kadın kısırlığı
0.1 mg triptorelin reçete etmeden önce, hastanın hamile olmadığının doğrulanması gerekir.
GnRH analoglarının ve gonadotropinlerin kullanımıyla indüklenen foliküler stimülasyon, özellikle Polikistik Over Sendromu durumunda, yatkın hastaların azınlıkta önemli ölçüde arttırılabilir.
Decapeptyl - gonadotropin kombinasyonuna yumurtalık yanıtı, aynı dozda bile bir hastadan diğerine ve bazı durumlarda aynı hastada bir döngüden diğerine değişebilir.
Ovulasyon düzenli klinik ve biyolojik kontrollerle yakından izlenmelidir: ultrason muayeneleri ve plazma östrojenlerinin değerlendirilmesi
Diğer GnRH analoglarında olduğu gibi, gonadotropinlerle kombinasyon halinde triptorelin kullanımıyla ilişkili ovaryan hiperstimülasyon sendromu (OHSS) raporları olmuştur.
Predispoze hastalarda meydana gelebilecek over hiper-yanıtı durumunda veya overin polikistik hastalığı durumunda, gonadotropin uygulamasının durdurulması tavsiye edilirken, Decapeptyl 0.1 mg uygulamasına birkaç gün devam edilir. olası bir spontan LH dalgalanması.
04.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim biçimleri
Triptorelin, gonadotropinlerin hipofiz salgısını etkileyen diğer ilaçlarla birlikte uygulandığında dikkatli olunmalıdır. ve tavsiye edilir hastanın hormonal durumu izlenir.
04.6 Hamilelik ve emzirme
Gebelik
GnRH agonistlerinin birlikte kullanımı teorik bir düşük veya fetal anormallik riski ile ilişkili olduğundan, triptorelin hamilelik sırasında kullanılmamalıdır. adet döngüsü dönene kadar tedavi.
Triptorelin infertilite tedavisi için kullanılmadan önce gebelik ekarte edilmelidir.Bu durumda triptorelin kullanıldığında, triptorelin ile oosit gelişimindeki sonraki anormallikler arasında nedensel bir ilişki olduğunu gösteren klinik kanıt yoktur. gebelik.
Besleme zamanı
Triptorelin emzirme döneminde kullanılmamalıdır.
04.7 Araç ve makine kullanma yeteneği üzerindeki etkiler
Araç ve makine kullanma yeteneği üzerindeki etkiler üzerine herhangi bir çalışma yapılmamıştır. Bununla birlikte, triptorelin farmakolojik profili göz önüne alındığında, triptorelinin hastanın araç veya makine kullanma yeteneği üzerinde muhtemelen hiçbir etkisi yoktur veya ihmal edilebilir düzeydedir.
04.8 İstenmeyen etkiler
GnRH analogları alan hastalarda artmış lenfosit sayıları bildirilmiştir.
Klinik çalışmalarda deneyim
Klinik çalışmalara katılan ve hızlı salimli formülasyon olan triptorelin ile tedavi edilen yetişkin popülasyonda, 3 ay boyunca günlük tedavi edilen prostat kanserli 127 erkek ve in vitro fertilizasyon protokolleri uygulanan yaklaşık 1.000 kadın yer aldı. Erkeklerde ve kadınlarda 3.75 mg ve 11.25 mg triptorelin formülasyonları ile gerçekleştirilen klinik deneyler sırasında kazanılan ayrıntılı güvenlik deneyimi de dahil edilmiştir.
Klinik çalışmalardan elde edilen güvenlik deneyiminin genel analizi, hipogonadotropik hipogonadizm veya bazen ilk hipofiz-gonadal stimülasyonun bir sonucu olarak ilaç sınıfına bağlı advers reaksiyonları içermiştir.
Advers reaksiyonların sıklığı şu şekilde sınıflandırılmıştır: çok yaygın (≥1/10) - Yaygın (≥1/100-
Yetişkinlerde genel tolere edilebilirlik
Çok yaygın: Genellikle tedavinin kesilmesini gerektirmeyen hafif ila şiddetli sıcak basmaları.
Yaygın: Psikiyatrik bozukluklar (ruh hali değişiklikleri, depresyon) *
Yaygın olmayan: psikiyatrik bozukluklar (ruh hali değişiklikleri, depresyon) **
* Uzun süreli kullanım. Bu frekans, tüm GnRH agonistlerinde ortak olan sınıf etkisinin frekansına dayanmaktadır.
** Kısa süreli kullanım. Bu frekans, tüm GnRH agonistlerinde ortak olan sınıf etkisinin frekansına dayanmaktadır.
Kadınlarda genel tolere edilebilirlik
Tedavinin başlangıcında çok yaygın: infertilite tedavisinde, gonadotropinlerle birlikte kullanıldığında triptorelin over hiperstimülasyon sendromuna neden olabilir.Ovaryan hipertrofi, dispne, pelvik ve/veya karın ağrısı oluşabilir (bkz. bölüm 4.4).
Aylık ve üç aylık formülasyonlarda tritorelin ile tedavinin başlangıcında çok yaygın:
menoraji veya metroraji dahil olmak üzere genital kanama ilk enjeksiyonu takip eden ayda meydana gelebilir.
Aylık ve üç aylık formülasyonlarda tritorelin tedavisi sırasında çok yaygın:
bu advers reaksiyonlar, uyku bozuklukları, baş ağrısı, duygudurum değişikliği, vulvo-vajinal kuruluk ve disparoni, libido azalması gibi hipofiz-yumurtalık bloğu ile ilgili bir dizi hipo-östrojenik olayı gösterir.
Aylık formülasyonda tritorelin ile tedavi sırasında yaygın:
göğüs ağrısı, kas spazmları, artralji, kilo alımı, bulantı, karında rahatsızlık/ağrı, asteni. Uzun süreli kullanımda ruh hali değişiklikleri ve depresyon bildirilmiştir.
Yerel tolere edilebilirlik
Çok seyrek: Enjeksiyon bölgesinde ağrı, eritem ve iltihaplanma.
Pazarlama sonrası bilgiler
Pazarlama sonrası gözetim sırasında IVF tedavisi gören kadınlarda başka istenmeyen etkiler bildirilmiştir. İstenmeyen etkiler, sistemik organik kategorilere göre ve bildirilen etkilerin azalan sıklık sırasına göre sınıflandırılır:
Deri ve deri altı doku bozuklukları: kaşıntı, kurdeşen, döküntü, anjiyonörotik ödem dahil aşırı duyarlılık reaksiyonları ("Kontrendikasyonlar" bölümüne bakın)
Sinir sistemi bozuklukları: baş ağrısı
Göz bozuklukları: bulanık görme veya görme bozuklukları bölümleri.
04.9 Doz aşımı
Doz aşımının bir sonucu olarak herhangi bir advers reaksiyon bildirilmemiştir.
Hayvandaki toksikolojik verilere dayanarak, üreme sistemi üzerinde sonuçları olan seks hormonlarının konsantrasyonu üzerindeki etkilerden başka hiçbir etki öngörülemez. Doz aşımı durumunda semptomatik tedavi önerilir.
05.0 FARMAKOLOJİK ÖZELLİKLER
05.1 Farmakodinamik özellikler
Farmakoterapötik grup: endokrin tedavisi; gonadotropin salgılatıcı hormon analogları
ATC kodu: L02AE04
Triptorelin, doğal peptidin analoğu olan sentetik bir dekapeptittir (D-Trp-6-LHRH). 6. pozisyonda glisinin D-triptofan ile ikame edilmesi, dikkate değer bir agonist güç ve enzimatik bozulmaya karşı daha belirgin bir direnç sağlar.
Triptorelin, çeşitli in vitro ve in vivo çalışmalarda, deneysel modele bağlı olarak, doğal nöropeptidden 100 kata kadar daha fazla değişken bir potansiyel göstermiştir. Hayvanlarda ve kadınlarda yapılan araştırmalar, gonadotropinlerin [(FSH ve LH) salgılanmasının kısa bir stimülasyonu aşamasından sonra - bunun sonucunda östradiol salgılanmasının - yaklaşık bir hafta süren] triptorelin uygulamasının, baskılama ile engelleyici bir etki uyguladığını göstermiştir. yumurtalık fonksiyonu.
Triptorelin, gonadotropinler tarafından indüklenen folikülojenezin daha iyi kontrolüne izin vererek, intercurrent LH piklerinin baskılanmasını sağlar. Bu, foliküler işe alımda bir artışın yanı sıra üretilen embriyoların sayısında ve döngü başına gebeliklerde bir artışa dönüşür.
05.2 Farmakokinetik özellikler
Sağlıklı gönüllülerde: subkutan uygulamadan sonra triptorelin (0.1 mg) hızla emilir (1.85 ± 0.23 ng / ml'ye eşit plazma zirvesi, 0.63 ± 0.26 saat sonra ulaşılır). 3-4 saat süren dağıtım aşaması, 1562.7 ± 158.8 ml / kg'a eşdeğer bir dağılım hacmiyle sonuçlanır. Eliminasyon, 7,6 ± 1,6 saatlik biyolojik yarılanma ömrü ile gerçekleşir ve toplam plazma klirensi 161,7 ± 28,6 ml/dk'dır.
05.3 Klinik öncesi güvenlik verileri
Akut toksisite, sıçanlarda ve farelerde intraperitoneal ve subkutan olarak değerlendirildi.
İntraperitoneal yolla ilgili olarak, LD50 çok düşüktür ve sıçanda 100 mg/kg'a eşittir, farede ise 160-200 mg/kg'a eşittir.
Deri altı uygulamayı takiben, her iki türde de LD50, olağan terapötik doza kıyasla önemli ölçüde daha yüksek dozlarda (sıçanlarda 150.000 kez ve farede 250.000 kez) ölçülebilir değildir.
Kronik toksisite çalışmaları, tekrarlanan uygulamaların üreme dışındaki organ ve sistemlerde değişikliklere neden olmadığını göstermiştir. Hayvan çalışmaları teratojenik etkiler göstermedi.
06.0 FARMASÖTİK BİLGİLER
06.1 Yardımcı maddeler
Mannitol, Sodyum klorür, Enjeksiyonluk su
06.2 Uyumsuzluk
Diğer ilaçlarla uyumsuzluk verisi yoktur.
06.3 Geçerlilik süresi
Sağlam ambalajında 24 ay.
06.4 Depolama için özel önlemler
Özel saklama koşulları yok
06.5 İç ambalajın yapısı ve paketin içeriği
7 şişe toz ve 1 ml'lik 7 çözücü şişe paketi
06.6 Kullanım ve kullanım talimatları
Hiçbiri
07.0 PAZARLAMA YETKİ SAHİBİ
IPSEN S.p.A. - Via A. Figino 16 - Milano.
08.0 PAZARLAMA YETKİ NUMARASI
026999045
09.0 İLK İZİN VEYA İZİNİN YENİLENMESİ TARİHİ
İlk izin tarihi: 08.05.1996
Son yenileme tarihi: 01.12.2009
10.0 METİN REVİZYON TARİHİ
2 Nisan 2014 tarihli V&A 674 Tespiti