Aktif maddeler: Dallı zincirli amino asitler
SIFRAMIN 40 mg/ml İNFÜZYON ÇÖZELTİSİ
Siframin neden kullanılır? Bu ne için?
SIFRAMIN, insan vücudu için gerekli olan ve ağız yoluyla beslenemeyen hastaların beslenmesinde (parenteral beslenme) kullanılan amino asitler adı verilen bir grup madde içerir.
Bu ilacın, ciddi karaciğer hasarının (karaciğer koması) neden olduğu bir komadan uyanmak için protein maddelerini desteklediği belirtilmiştir.
Kontrendikasyonlar Siframin ne zaman kullanılmamalıdır?
SIFRAMIN'i KULLANMAYINIZ
- Bir veya daha fazla amino aside veya bu ilacın diğer bileşenlerinden herhangi birine alerjiniz varsa (bölüm 6'da listelenmiştir);
- Amino asitleri metabolize etmekte sorun yaşıyorsanız;
- Böbrek fonksiyonunuzla ilgili ciddi sorunlarınız varsa (böbrek yetmezliği).
Kullanım Önlemleri Siframin almadan önce bilmeniz gerekenler
SIFRAMIN'i kullanmadan önce doktorunuz, eczacınız veya hemşireniz ile konuşunuz.
SIFRAMIN ile tedaviniz sırasında, doktorunuz mineral tuz düzeylerini (hidroelektrolitik denge) ve kanın pH'ını (asit-baz dengesi) kontrol etmek için sizi özel laboratuvar analizlerine tabi tutacak ve gerekirse solüsyonlar vererek dengeyi yeniden sağlayacaktır. Ayrıca doktorunuz gerekli görürse midenizi korumaya yönelik ilaçlar (H2 antagonistleri) yazacaktır.
Şeker hastalığınız varsa, doktorunuz tükettiğiniz şeker miktarını (kalori alımını) izleyecektir.
Etkileşimler Hangi ilaçlar veya yiyecekler Siframin'in etkisini değiştirebilir?
Başka ilaçlar kullanıyorsanız, yakın zamanda kullandıysanız veya kullanabilecekseniz doktorunuza, eczacınıza veya hemşirenize söyleyiniz.
Diğer ilaçlarla bilinen bir etkileşimi yoktur.
Uyarılar Şunları bilmek önemlidir:
Hamilelik ve emzirme
Hamileyseniz veya emziriyorsanız, hamile olabileceğinizi düşünüyorsanız veya bebek sahibi olmayı planlıyorsanız bu ilacı kullanmadan önce doktorunuza veya eczacınıza danışınız.
Araç ve makine kullanma
İlgili değil.
Dozaj ve kullanım yöntemi Siframin nasıl kullanılır: Dozaj
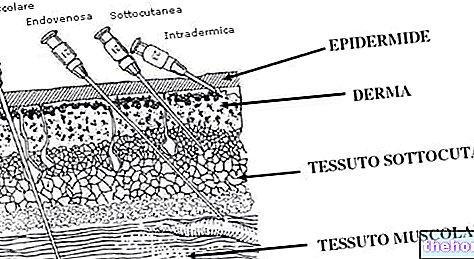
Bu ilaç size bir doktor veya diğer eğitimli personel tarafından 24 saatlik bir süre içinde yavaş infüzyon (damardan damlama) şeklinde verilecektir.Emin değilseniz doktorunuza, eczacınıza veya hemşirenize danışın.
Önerilen doz, tedavinin ilk günü için 1000 ml çözeltidir, daha sonra ikinci ve sonraki günlerde 1500 ml'ye yükseltilecektir, 500 ml'lik bir şişenin içeriğinin size doğrudan yavaş infüzyonla verileceği unutulmamalıdır. yaklaşık 8 saat süren bir damara (intravenöz yolla). Aynı zamanda size %50-70 oranında yeterli miktarda glikoz verilecektir (24 saatte yaklaşık 300-400 gr).
Çözelti yalnızca berraksa, görünür parçacıklardan arındırılmışsa ve kap sağlamsa kullanılmalıdır.
Aşırı doz: Çok fazla Siframin aldıysanız ne yapmalısınız?
Size çok fazla SIFRAMIN verildiğini düşünüyorsanız, derhal doktorunuza veya başka bir sağlık uzmanına bildirin.
Bu ilacın kullanımıyla ilgili başka sorularınız varsa, doktorunuza, eczacınıza veya hemşirenize sorunuz.
Yan Etkiler Siframin'in yan etkileri nelerdir?
Tüm ilaçlar gibi, bu ilaç da yan etkilere neden olabilir, ancak bunları herkes almayabilir.
SIFRAMIN kullanıldıktan sonra istenmeyen etkiler bildirilmemiştir.
Yan etkilerin raporlanması
Herhangi bir yan etki yaşarsanız, doktorunuzla veya eczacınızla konuşun.Bu broşürde listelenmeyen olası yan etkiler de buna dahildir. Ayrıca yan etkileri doğrudan www.agenziafarmaco.gov.it/it/responsabili adresindeki ulusal raporlama sistemi aracılığıyla da bildirebilirsiniz.Yan etkileri bildirerek bu ilacın güvenliği hakkında daha fazla bilgi sağlamaya yardımcı olabilirsiniz.
Son Kullanma ve Saklama
Bu ilacı çocukların göremeyeceği ve erişemeyeceği bir yerde saklayın.
Bu ilacı, karton üzerinde belirtilen "EXP" den sonra belirtilen son kullanma tarihinden sonra kullanmayınız.
Son kullanma tarihi, o ayın son gününü ifade eder.
25 °C'nin altında saklayınız. Soğutmayın veya dondurmayın.
İlacı ışıktan korumak için orijinal ambalajında saklayınız.
Herhangi bir ilacı atık su veya evsel atık yoluyla atmayın.Artık kullanmadığınız ilaçları nasıl atacağınızı eczacınıza sorun.Bu çevrenin korunmasına yardımcı olacaktır.
Son tarih "> Diğer bilgiler
SIFRAMIN'in içindekiler
- Aktif bileşenler dallı zincirli L-amino asitlerdir. 1000 ml çözelti, 12.5 g Lisolösin, 15.5 g L-lösin, 12.0 g L-valine karşılık gelen 40 g toplam amino asit içerir. Her litre çözelti 4.42 g toplam nitrojen içerir. pH 5.8-6.8.
- Diğer bileşen enjeksiyonluk sudur.
SIFRAMIN'in neye benzediğinin ve paketin içeriğinin açıklaması
100 ml, 250 ml, 500 ml, 20x500 ml, 1000 ml'lik şişe.
Kaynak Paket Broşürü: AIFA (İtalyan İlaç Ajansı). Ocak 2016'da yayınlanan içerik. Mevcut bilgiler güncel olmayabilir.
En güncel sürüme erişmek için AIFA (İtalyan İlaç Ajansı) web sitesine erişmeniz önerilir. Sorumluluk reddi ve faydalı bilgiler.
01.0 TIBBİ ÜRÜNÜN ADI -
SIFRAMIN 40 MG/ML İNFÜZYON ÇÖZÜMÜ
02.0 KALİTATİF VE KANTİTATİF BİLEŞİM -
1000 ml çözelti şunları içerir:
Yardımcı maddelerin tam listesi için bölüm 6.1'e bakın.
03.0 FARMASÖTİK FORM -
İnfüzyon için çözüm.
04.0 KLİNİK BİLGİLER -
04.1 Terapötik endikasyonlar -
Sadece hepatik komadan uyanmak için dallı amino asitlerin yavaş sürekli perfüzyonunda parenteral tedarik.
04.2 Pozoloji ve uygulama yöntemi -
İntravenöz infüzyon için. Çözelti, tedavinin ilk gününde 1000 ml'lik dozlarda uygulanmalıdır, ikinci gün ise 500 ml'lik bir şişenin içeriğinin 8 saatte infüze edilmesi gerektiği akılda tutularak 1500 ml'ye ulaşılması önerilir. %50-70 Glikoz karışım solüsyonunun yeterli miktarda (24 saatte 300-400 g) demlenmesi gerekir.
İnfüzyon, yavaş bir infüzyonla 24 saat içinde verilmelidir.
Yavaş damlama yönetimi için kullanın.
04.3 Kontrendikasyonlar -
Etkin madde(ler)e veya bölüm 6.1'de listelenen yardımcı maddelerden herhangi birine karşı aşırı duyarlılık.
Bireysel amino asitlerin metabolizmasındaki bozukluklar, böbrek yetmezliği.
04.4 Özel uyarılar ve uygun kullanım önlemleri -
H2-antagonistlerinin profilaktik olarak uygulanmasının gerekip gerekmediği araştırılmalıdır.
Genel olarak, özellikle daha ciddi durumlarda, gerekirse elektrolitik düzeltmelerin uygulanması için hidroelektrolitik denge ve asit-baz dengesi üzerinde kontrollerin yapılması tavsiye edilir.
Özellikle şeker hastalarında kalori alımına gereken önem verilmelidir.
Yalnızca çözelti berraksa, görünür asılı parçacıklardan arındırılmışsa ve kap sağlamsa kullanın.
Işıktan koruyun ve 25 °C'yi geçmeyen bir sıcaklıkta saklayın.
Çocukların erişemeyeceği yerlerde saklayın.
04.5 Diğer tıbbi ürünlerle etkileşimler ve diğer etkileşim biçimleri -
Diğer ilaçlarla bilinen herhangi bir reaksiyon yoktur. Ancak infüze edilecek solüsyona ilaç veya diğer besin maddelerinin eklenmesinden kaçınılmalıdır.
04.6 Hamilelik ve emzirme -
Ürünün hamilelik sırasında kullanımına ilişkin şu anda herhangi bir bilgi mevcut değildir.
04.7 Araç ve makine kullanma yeteneği üzerindeki etkiler -
İlgili değil.
04.8 İstenmeyen etkiler -
İnfüzyonlar talimatlara göre ve bireysel hastaların durumunun dikkatli bir şekilde değerlendirilmesiyle uygulandığında ikincil nitelikteki belirtiler.
Şüpheli advers reaksiyonların raporlanması
İlacın ruhsatlandırılmasından sonra meydana gelen şüpheli advers reaksiyonların raporlanması, tıbbi ürünün fayda/risk dengesinin sürekli olarak izlenmesine imkan verdiği için önemlidir. Sağlık profesyonellerinden şüpheli advers reaksiyonları ulusal raporlama sistemi aracılığıyla bildirmeleri istenir. "adres http: //www.agenziafarmaco.gov.it/it/responsabili.
04.9 Doz aşımı -
Özel bir prosedür yok
05.0 FARMAKOLOJİK ÖZELLİKLER -
05.1 "Farmakodinamik özellikler -
Farmakoterapötik grup: amino asitler, parenteral beslenme için çözelti, ATC kodu: B05BA01.
SIFRAMIN, hepatik komadan uyanmada temel bir terapötik etki oynayan ve geleneksel tedavilerle (laktuloz, neomisin, vb.).
05.2 "Farmakokinetik özellikler -
İntravenöz infüzyonla sağlanan dallı zincirli amino asitler, enteral beslenmeyle sağlanan amino asitlerinkiyle karşılaştırılabilir bir farmakokinetik profile sahiptir.
05.3 Klinik öncesi güvenlik verileri -
i.v. tavşanlarda, 40 ml / kg ürün (maksimum terapötik günlük dozun 1.33 katına eşit), kan basıncında, solunum hızında ve periferik sinir sistemi fonksiyonunda herhangi bir önemli değişiklik indüklememiştir.
Yetersiz beslenen sıçanda, i.p. 20 gün boyunca 30 ml / kg ürün (maksimum terapötik günlük doza eşit), kontrollere kıyasla daha fazla kilo alımına ve hipoalümentasyondan ölüm oranında bir azalmaya neden oldu.
Kobayda 27 gün arayla arka arkaya iki kez uygulanan aynı doz (ilki i.p. yolu ile ve ikincisi i.v. yolu ile) anafilaktik sendromun özelliği olan ani veya geç semptomlar üretmedi. Aynı doz i.v. tavşanda art arda (12 ardışık gün) dolaşımdaki antikorların görünümünü indüklemedi. Daima aynı doz i.v. gine domuzunda gün aşırı yedi kez kompleman fiksasyon testi değişmedi. Bu son üç testin sonuçlarından, ürünün herhangi bir immünojenik aktivitesi laboratuvar hayvanında hariç tutulmuştur.
Toksikolojik açıdan, yapılan çalışmaların sonuçları tamamen güven vericidir.Tek uygulama için toksisite testlerinde, spesiyalite ip sıçanda 10 ila 60 ml / kg dozlarda ve tavşanda iv olarak dozlarda kullanılmıştır. Tedavi edilen hayvanlarda herhangi bir ölüm vakasına neden olmadan 20 ila 50 ml / kg (yani maksimum günlük terapötik dozun 2 katına kadar). 0.25 ila 1 maksimum terapötik günlük doz, tedavi edilen hayvanlarda ölüm veya belirli toksik semptomlar yoktu belli olmak.
Son olarak, ürün sıçan ve tavşanların gebelik ve embriyofetal gelişimi üzerinde herhangi bir olumsuz etkiye neden olmamıştır.
06.0 FARMASÖTİK BİLGİLER -
06.1 Yardımcı maddeler -
su p.p.i.
06.2 Uyumsuzluk "-
Bilinmeyen.
06.3 Geçerlilik süresi "-
2 yıl
06.4 Depolama için özel önlemler -
İlacı ışıktan korumak için orijinal ambalajında saklayınız. 25 °C'nin üzerinde saklamayın.
06.5 İç ambalajın niteliği ve paketin içeriği -
100-250-500-1000 ml'lik şişeler.
Tüm paket boyutları pazarlanmayabilir
06.6 Kullanım ve kullanım talimatları -
Kullanılmayan ilaçlar ve bu ilaçtan kaynaklanan atıklar yerel yönetmeliklere uygun olarak atılmalıdır.
07.0 "PAZARLAMA İZNİ" SAHİBİ -
Fresenius Kabi Italia S.r.l.
Via Camagre, 41 - 37063 Isola della Scala (VR)
08.0 PAZARLAMA YETKİ NUMARASI -
Şişe 100 ml A.I.C. numara 029165014
Şişe 250 ml A.I.C. numara 029165026
Şişe 500 ml A.I.C. numara 029165038
1000 ml şişe A.I.C. n ° 029165040
20 şişe 500 ml A.I.C. numara 029165053
09.0 İLK İZİN VEYA İZİNİN YENİLENMESİ TARİHİ -
15 Kasım 1994 / 15 Kasım 2009.
10.0 METİN REVİZYON TARİHİ -
Kasım 2015