LÜTFEN AKLINIZDA BULUNDURUN: TIBBİ ÜRÜN ARTIK İZİN VERİLMEMEKTEDİR
Leflunomid Teva nedir?
Leflunomid Teva, etkin madde olarak leflunomid içeren bir ilaçtır ve tabletler halinde mevcuttur (yuvarlak beyaz 10 mg; üçgen koyu bej 20 mg).
Leflunomide Teva 'jenerik' bir ilaçtır, yani Leflunomide Teva, Avrupa Birliği'nde (AB) Arava adı verilen bir 'referans ilaca' benzerdir.
Leflunomid Teva ne için kullanılır?
Leflunomid Teva, aktif romatoid artritli (bağışıklık sisteminin eklemlerde iltihaplanmaya neden olan bir hastalığı) olan yetişkinleri tedavi etmek için kullanılır.
İlaç sadece reçete ile alınabilir.
Leflunomid Teva nasıl kullanılır?
Leflunomid Teva tedavisi, romatoid artrit tedavisinde deneyimli bir uzman tarafından başlatılmalı ve gözetiminde yapılmalıdır.Doktor, Leflunomid Teva'yı reçete etmeden önce ve tedavi sırasında düzenli olarak hastanın karaciğer, beyaz kan hücresi ve trombosit sayılarını kontrol etmek için kan testleri yapmalıdır.
Leflunomid Teva tedavisi, üç gün boyunca günde bir kez 100 mg'lık bir 'yükleme dozu' ile başlatılmalı ve ardından bir idame dozu uygulanmalıdır.Önerilen idame dozu günde bir kez 10-20 mg'dır. İlaç genellikle dört ila altı hafta sonra çalışmaya başlar. Etki, altı aya kadar daha da iyileşebilir.
Leflunomid Teva nasıl çalışır?
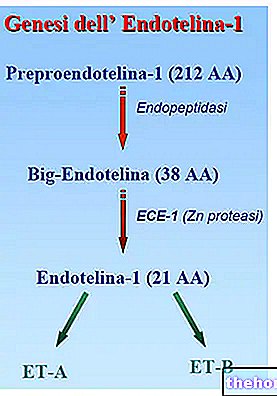
Leflunomid Teva'daki aktif madde, leflunomid, bir immünosupresandır. Bu madde, iltihaplanmadan sorumlu olan 'lenfositler' adı verilen bağışıklık hücrelerinin üretimini azaltarak iltihabı azaltır. Leflunomid bunu, lenfositlerin çoğalması için gerekli olan 'dihidroorotat dehidrojenaz' adı verilen bir enzimi bloke ederek yapar. Daha az lenfosit ile inflamasyon azalır ve artrit semptomlarının kontrolüne yardımcı olur.
Leflunomid Teva nasıl çalışılmıştır?
Leflunomid Teva jenerik bir ilaç olduğundan, hastalardaki çalışmalar, referans ilaç Arava ile biyoeşdeğerliğini doğrulamakla sınırlıydı. İki ilaç, vücuda bir kez girdiklerinde, aynı düzeyde aktif bileşen sağlıyorsa biyoeşdeğerdir.
Leflunomid Teva ile ilişkili riskler ve faydalar nelerdir?
Leflunomid Teva jenerik bir ilaç olduğundan ve referans ilaca biyoeşdeğer olduğundan, bununla ilişkili fayda ve risklerin referans ilaçla aynı olduğu kabul edilir.
Leflunomid Teva neden onaylandı?
CHMP (İnsan Kullanımına Yönelik Tıbbi Ürünler Komitesi), AB gereklilikleri uyarınca, Leflunomid Teva'nın Arava ile niteliksel olarak karşılaştırılabilir ve biyoeşdeğer olduğunun gösterildiği sonucuna varmıştır ve bu nedenle, Arava örneğinde olduğu gibi, faydaların tanımlananlardan daha ağır bastığı sonucuna varmıştır. Komite, Leflunomid Teva'ya pazarlama izni verilmesini tavsiye etti.
Leflunomid Teva ile ilgili diğer bilgiler
10 Mart 2011'de Avrupa Komisyonu TEVA Pharma B.V. Leflunomid Teva için Avrupa Birliği genelinde geçerli bir "Pazarlama İzni" Bu yetki beş yıl süreyle geçerlidir ve yenilenebilir.
Bu özetin son güncellemesi: 01-2011.
Bu sayfada yayınlanan Leflunomide Teva ile ilgili bilgiler güncelliğini yitirmiş veya eksik olabilir. Bu bilgilerin doğru kullanımı için Sorumluluk Reddi ve faydalı bilgiler sayfasına bakın.













----tiamfenicolo.jpg)