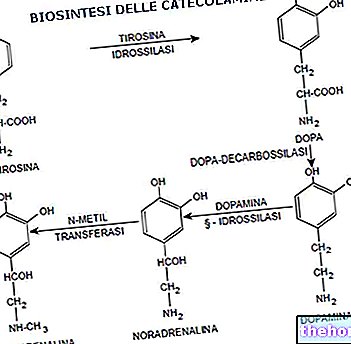
Amino asitler ve proteinler, mineral dünyasından canlı maddeye geçişin ara maddeleridir.
Adlarından da anlaşılacağı gibi, amino asitler iki işlevli organik maddelerdir: amino işlevi (-NH2) ve karboksil işlevinden (-COOH); amino grubunun karboksi grubuna göre işgal ettiği konuma bağlı olarak α, β, γ, vb. olabilirler:



Biyolojik olarak önemli amino asitlerin tümü α-amino asitlerdir.
Protein yapıları yirmi amino asitten oluşur.
Yukarıda gösterilen jenerik yapılardan görülebileceği gibi, amino asitlerin hepsinin ortak bir kısmı ve onları karakterize eden farklı bir kısmı vardır (jenerik olarak R ile temsil edilir).
Yirmi amino asitten on dokuzu optik olarak aktiftir (polarize ışık düzlemini saptırırlar).
Çoğu amino asit, yalnızca bir amino grubu ve bir karboksil içerir, bu nedenle denir. nötr amino asitler; fazla karboksil içerenlere denir asit amino asitler fazladan bir amino grubuna sahip olanlar ise bazik amino asitler.
Amino asitler kristal katılardır ve suda iyi çözünürlüğe sahiptirler.
Diyette bazı amino asitlerin eksikliği, gelişimde ciddi değişikliklere neden olur; aslında insan organizması tam olarak esansiyel olarak adlandırılan (beslenmeyle birlikte alınması gereken) bazı amino asitleri sentezleyemezken, kendi başına sadece bazı amino asitleri (esansiyel olmayanlar) üretebilir.
Esansiyel amino asitlerin eksikliğinden kaynaklanan hastalıklardan biri, kwashiorkor (Afrika lehçesinden gelen ve "birinci ve ikinci" anlamına gelen bir kelime) adıyla bilinen hastalıktır; bu hastalık ilk çocuğu etkiler, ancak ikinci çocuğun doğumundan sonra, çünkü ilk çocuk doğru protein kaynağı içeren anne sütünden yoksundur. Bu nedenle, bu hastalık, yetersiz beslenen popülasyonlar arasında yaygındır ve ishal, yani organizmanın ilerleyici bir zayıflamasına yol açan iştahsızlık içerir.
Daha önce belirtildiği gibi, doğal amino asitler, glisin hariç (R grubu yerine hidrojenli bir a-amino asittir ve yirminin en küçüğüdür), en az bir asimetrik varlığın varlığından dolayı optik aktiviteye sahiptir. karbon. Doğal amino asitlerde sadece amino ve karboksi gruplarının bağlı olduğu asimetrik karbonun mutlak konfigürasyonu L serisine aittir;
D-amino asitler asla bir proteinin yapısının parçası olmazlar.
Şunu hatırlıyoruz:
DNA ---- transkripsiyon → m-RNA ---- translasyon → protein
Transkripsiyon, L-amino asitler olarak kodlama yeteneğine sahiptir; D-amino asitler protein olmayan yapılarda bulunabilir (örn. bakterilerin astar duvarında: bakterilerde koruyucu bir rol için D-amino asitlere sahip olmak için genetik bilgi yoktur, ancak enzimler için genetik bilgi vardır" bakteri astar duvarı ile ilgilenen).
Amino asitlere geri dönelim: R grubunun farklı yapısı, her amino asidin bireysel özelliklerini tanımlar ve proteinlerin özelliklerine belirli bir katkı sağlar.
Bu nedenle amino asitleri R grubunun doğasına göre bölmek düşünüldü:
Polar fakat yüksüz amino asitler:
Glisin (R = H-)
Serin (R = HO-CH2-)
treoningerekli
Treonin iki simetri merkezine sahiptir: Doğada sadece 2S, 3R treonin bulunur.
Treonin esansiyel bir amino asittir (vazgeçilmez ile karıştırılmamalıdır: tüm amino asitler esansiyeldir), bu nedenle diyetle, yani onu içeren yiyecekleri yiyerek alınmalıdır, çünkü daha önce belirtildiği gibi, genetik miras mevcut değildir. insan hücreleri bu amino asidi üretebilir (bu miras birçok bitkide ve daha iyilerde bulunur).
Serin ve treoninin hidroksil grubu, bir fosforil grubuyla (fosfoserin ve fosfotreonin elde ederek) esterlenebilir, bu işleme denir. fosforilasyon; fosforilasyon, doğada hücrenin içi ve dışı arasındaki sinyallerin çevrilmesi için kullanılır.
Sistein (R = HS-CH2-)
Sisteinin sülfhidrili, serinin hidroksilinden daha kolay protonlanabilir: kükürt ve oksijen, altıncı grubun her ikisidir, ancak kükürt, daha büyük boyutlara sahip olduğu için daha kolay oksitlenebilir.
Tirozin [R = HO- (C6H4) -CH2-]
not
(C6H4) = di-ikameli benzen halkası
Serin ve treonin ile olduğu gibi, hidroksil de esterlenebilir (fosforile edilebilir).Asparagin (R = NH2-CO-CH2-)
Glutamin (R = NH2-CO-CH2-CH2-)
Polar olmayan amino asitler
hidrofobik yan gruplara sahiptir; Bu sınıf içinde şunları ayırt ederiz:
Alifatikler:
Alanin (R = CH3-)
Valin (R = (CH3) 2-CH-) gerekli
Lösin (R = (CH3) 2-CH-CH2-) esansiyel
İzolösin (R =
) gerekli
Metionin (R = CH3-S-CH2-CH2-) esansiyel
Hücre zarları, hidrofobik karakterleri sayesinde sabitlenmiş proteinlerle bir lipid çift tabakasından oluşur, bu nedenle alanin, valin, izolösin ve lösin içerirler. Metionin ise hemen hemen her zaman küçük miktarlarda (yaklaşık %1) bulunan bir amino asittir.
prolin
Aromatik:
Fenilalanin (R = Ph-CH2-) Ph = fenil: temel tek ikameli benzen
Triptofan (R =
gerekli
Aromatik olan bu iki amino asit, yakın ultraviyole radyasyonu (yaklaşık 300 nm) emer; bu nedenle, bu amino asitleri içeren bilinen bir proteinin konsantrasyonunu belirlemek için UV spektrofotometrisi tekniğinden yararlanmak mümkündür.
Yüklü amino asitler
Sırayla ayrılırlar:
Asidik amino asitler (pH 7'de negatif yüklü polar kalıntılara sahip) böyledir çünkü pozitif bir H + yükü verebilirler:
Aspartik asit
Glutamik asit (R =
)
Bu amino asitler sırasıyla asparagin ve glutaminden türetilir; dördü de doğada mevcuttur ve bu demek oluyor ki c "her biri için özel bir bilgidir, yani c" DNA'da her birini kodlayan bir baz üçlüsüdür.
Bazik amino asitler (pH 7'de pozitif yüke sahip polar kalıntılara sahip) böyledir çünkü pozitif bir H + yükünü kabul edebilirler:
Lizin (R =
) gerekli
Arginin (R =
)
Histidin (R =
)
Yan zincirlerinde amino asit türevlerinin bulunduğu proteinler vardır: örneğin, bir fosfoserin mevcut olabilir (fosfoserin kodlayan genetik bilgi yoktur, sadece serin için olandır); fosfoserin bir modifikasyondur. çeviri sonrası: protein sentezi gerçekleştikten sonra
DNA ---- transkripsiyon → m-RNA ---- translasyon → protein
bu tür translasyon sonrası modifikasyonlar, proteinin yan zincirlerinde meydana gelebilir.
Ayrıca bakınız: Proteinler, kimyaya bir bakış