genellik
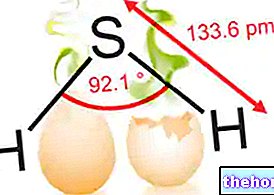
Hidrojen sülfür - hidrojen sülfür veya dihidrojen sülfür (H2S) olarak da bilinir - suda ve etanolde çözünür ve çok güçlü bir "çürük yumurta" kokusu yayan bir moleküldür.

Dihidrojen sülfür (H2S) insanlar için zehirli ve hatta ölümcüldür; havaya salınması esas olarak aşağıdakilerin bir sonucu olarak gerçekleşir:
- Sülfür içeren proteinlerin, disülfid köprüleri gibi stabilize edici bağlarda ve kükürt amino asitlerinde bakteriyel veya enzimatik ayrışması
- Disülfid köprülerinin kırılması ile proteinlerin pişirilmesi ve ikincil, üçüncül ve kuaterner yapıların denatürasyonu.
Hidrojen sülfür (H2S) aşağıdakilerden kaynaklanan ekshalasyonlarda yüksek oranda bulunur: toprak altı, ham petrol ve yüksek çürüme aktivitesine sahip alanlarda (göletler, bataklıklar ve bataklıklar gibi) hava cepleri; hidrojen sülfür, dışkı ve bağırsak gazında en çok bulunan aromatik bileşenlerden biridir. ancak büyük miktarlarda salınması, esas olarak gıda endüstrisinin üretim döngülerinde, suyun çamurla arıtılmasında, petrol arıtımı vb.
Not. Dihidrojen sülfür (H2S) gümüşle reaksiyona girer ve yüzeysel olarak termal banyolardan sonra yüzüklerde, küpelerde ve kolyelerde görülebilen siyah bir gümüş sülfür patinası oluşturur.
toksisite
Hidrojen sülfür (H2S) mitokondriyal solunumu inhibe ederek etki eden bir zehirdir, bu nedenle toksik etkisi vücutta aerobik metabolizmayı kullanan tüm hücreleri (kırmızı kan hücreleri hariç hemen hemen hepsini) etkiler; hidrojen sülfürün (H2S) en tehlikeli özelliği orta-yüksek konsantrasyonlarda havadaki dihidrojen sülfürün (H2S) varlığı için tek alarm zili olarak koku alma duyusal algısını etkisiz hale getirme yeteneğidir. Düşük konsantrasyonlarda ise hidrojen sülfür (H2S) mukoz membranlarda tahrişe, hiperventilasyona ve akciğer ödemine neden olur ve uzun süreli maruz kalma kronik yorgunluk, iştahsızlık, baş ağrısı, bilişsel ve hafıza bozukluklarına yol açar.
Hidrojen sülfür (H2S) milyonda 0,0047 kısım (insanların %50'si tarafından) konsantrasyonlarında zaten algılanabilirken, 10ppm art arda 8 saat maruziyetin ardından sağlığa zarar verme riski olmaksızın toksisitenin alt sınırını temsil eder; 1000 ppm dihidrojen sülfür (H2S) seviyelerine eşit seviyelerde tek bir nefesten sonra bile ani bir çökme olur.
Milyonda parça (ppm) cinsinden konsantrasyonlar
İnsan organizması üzerindeki etkisi
0,0047ppm
İnsanların %50'si için alt algı sınırı
<10ppm
Günde 8 saat sağlığa zarar vermeden maruz kalma sınırı
10-20ppm
Gözlerin gaz tarafından tahriş olduğu sınır
50-100ppm
Hücre hasarına neden olan konsantrasyon
100-150ppm
Koku alma sinirini felç eden konsantrasyon
320-530ppm
Akciğer ödemine neden olan konsantrasyon
530-1000ppm
Hiperventilasyona neden olan konsantrasyon
800ppm
5 "maruziyetten sonra insanların %50'sinin ölüm oranı için alt sınır
> 1000ppm
1 tek nefesten sonra boğulmaya neden olan minimum konsantrasyon
Gıdadaki hidrojen sülfür
Hidrojen sülfür (H2S), gaz halinde buharlaşma yoluyla salındığı gıdalarda üretilebilir; hidrojen sülfür (H2S), örneğin disülfit köprülerinin kırılması ve hidrojen iyonlarının toplanması gibi bazı kimyasal dönüşümlerin tipik bir türevidir ( "Proteinlerin pişirilmesini" (denatürasyon) takiben H +) Bu reaksiyon, albüminin kükürtünden başlayarak dihidrojen sülfür (H2S) üreten (uçucu olmasına rağmen, protein tarafından tutulan) katı kaynatılmış yumurtada iyi algılanabilir. kabuk), bombardıman anında gazı anında serbest bırakarak burun tarafından algılanabilir. Haşlanmış yumurtada, yumurta akının pişirilmesiyle açığa çıkan hidrojen sülfürün (H2S) yumurta sarısının demirli (yüzeysel) şelatlanmasından sorumlu olduğunu ve yumurta sarısının demir adı verilen bir tuzun üretilmesinden sorumlu olduğunu da hatırlıyoruz. demirli sülfür (FeS), artı iki hidrojen iyonu; kimyasal reaksiyon aşağıdaki gibidir:
H2S + Fe ++ → FeS + H2
Not. Demirli sülfür, sarıdaki demiri şelatlarken ve metabolik kullanımını kısmen engellerken, düşük konsantrasyonlarda zararsız olan, ancak yüksek dozlarda hafife alınmaması gereken bir bileşiktir.
Hidrojen sülfür (H2S) ayrıca aşağıdakiler arasındaki ayrımı kolaylaştıran bir bileşiktir: bozunma sürecindekilere kıyasla sağlıklı hayvan kaynaklı gıdalar; bu, hem proteinlerin sülfür köprülerine hem de kükürt amino asitleri, bunun sonucunda dihidrojen sülfür (H2S) sentezine yönelik kükürt salınımı ile. Not. Bu süreç tanınabilir özellikle kötü koruma nedeniyle zarar gören yumurta ve balıkların bozulmasında.