Vectibix nedir?
Vectibix, aktif madde panitumumab içeren infüzyon (damar içine damlama) için bir çözelti haline getirilmiş bir konsantredir.
Vectibix ne için kullanılır?
Vectibix, vücudun diğer bölgelerine yayılmış bir kalın bağırsak kanseri olan metastatik kolorektal kanserli hastaların tedavisinde endikedir.Vectibix, kanser hücrelerinde protein bulunan hastalarda tek başına (tek başına) kullanılır. yüzeylerinde epidermal büyüme faktörü reseptörü (EGFR) adı verilen ve bir gen içeren "KRAS"değişmedi. KRAS kanser hücrelerinde mutasyona uğradığında tümör büyümesini uyaran bir gendir. Vectibix, bir "floropirimidin" (örneğin, 5-florourasil), oksaliplatin ve irinotekan dahil antikanser ilaç kombinasyonları ile rejimler artık etkili olmadığında kullanılır.
İlaç sadece reçete ile alınabilir.
Vectibix nasıl kullanılır?
Vectibix ile tedavi, antikanser tedavilerinin kullanımında uzmanlaşmış bir doktor tarafından denetlenmelidir.Tedaviye ancak KRAS güvenilir yöntemler kullanan yeterli deneyime sahip bir laboratuvar tarafından değiştirilmemelidir.
Önerilen Vectibix dozu, iki haftada bir infüzyon olarak verilen 6 mg/kg vücut ağırlığıdır. Önerilen infüzyon süresi yaklaşık 60 dakikadır, ancak daha yüksek dozlar 90 dakika sürebilir.
Vectibix nasıl çalışır?
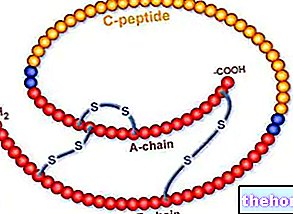
Vectibix'teki aktif madde, panitumumab, bir monoklonal antikordur. Monoklonal antikor, vücuttaki belirli hücrelerde bulunan belirli bir yapıyı (antijeni) tanımak ve bunlara bağlanmak için tasarlanmış bir antikordur (bir tür protein). Panitumumab, belirli hücrelerin yüzeyinde bulunan bir reseptör olan EGFR'ye bağlanmak için oluşturulmuştur. bazı kanserlerden gelen hücreler de dahil olmak üzere hücreler Sonuç olarak, kanser hücreleri artık EGFR tarafından iletilen büyümeleri, ilerlemeleri ve yayılmaları (metastaz) için gerekli mesajları almazlar. Panitumumab geni içeren kanser hücrelerinde çalışmıyor gibi görünüyor. KRAS mutasyona uğramış, çünkü bu tür hücrelerin büyümesi
EGFR aracılığıyla iletilen sinyaller tarafından kontrol edilir, böylece EGFR reseptörünün inhibisyonundan sonra bile büyümeye devam ederler.
Vectibix nasıl çalışılmıştır?
Vectibix'in etkileri, insanlarda incelenmeden önce deneysel modellerde test edildi.
Vectibix, önceki floropirimidin, oksaliplatin ve irinotekan tedavisi sırasında veya sonrasında hastalıkları kötüleşen kolon veya rektum kanserli toplam 463 hastayı içeren bir ana çalışmada incelenmiştir. En iyi destekleyici bakımla ilişkili "Vectibix'in etkinliği" tek başına "en iyi destekleyici bakım" ile karşılaştırıldı. En iyi destekleyici bakım, antibiyotikler, ağrı kesiciler, kan nakli ve ameliyat gibi hastaya yardımcı olabilecek herhangi bir ilaç veya tekniktir. diğer antikanser ilaçları hariç.Etkinliğin ana ölçüsü, hastalık kötüleşene veya hasta ölene kadar geçen süreydi. Çalışmanın sonuçları, tümörleri gen taşıyan 243 hastada ayrı ayrı analiz edildi. KRAS mutasyona uğramamış ve gen mutasyonu gözlenen 184 hastada KRAS.
Vectibix'in çalışmalar sırasında ne gibi yararları oldu?
Tümörlerin ortaya çıktığı hastalarda KRAS mutasyona uğramamışsa, Vectibix hastalık progresyonundan veya hasta ölümünden önceki zaman aralığını uzatmıştır: En iyi destek tedavisi ile birlikte Vectibix ile tedavi edilen hastalarda kaydedilen ortalama süre 12.3 hafta iken, tek başına en iyi destek tedavisi ile tedavi edilen deneklerde 7.3 hafta olmuştur. ile karakterize tümörleri olan hastalarda Vectibix'in olumlu bir etkisi yoktu. KRAS mutasyona uğramış: bu durumda, her iki hasta grubunda ilerleme veya ölüme kadar geçen ortalama zaman aralığı yaklaşık 7,3 haftaydı.
Vectibix ile ilişkili risk nedir?
Vectibix ile tedavi edilen hastaların yaklaşık %90'ı, çoğunlukla hafif ila orta dereceli cilt yan etkileri yaşar. Vectibix ile kaydedilen en yaygın yan etkiler (10 hastada 1'den fazlasında görülür) döküntü, akneiform dermatit (cildin akne benzeri iltihabı), eritem (ciltte kızarıklık), ciltte soyulma, kaşıntı, kuru cilttir. , çatlaklar cilt (ciltte çatlama), paronişi (tırnağı çevreleyen dokunun enfeksiyonu), ishal, yorgunluk, bulantı, kusma, hırıltı (nefes almada zorluk) ve öksürük. Vectibix ile bildirilen yan etkilerin tam listesi için paket broşürüne bakın.
Vectibix, panitumumab veya diğer bileşenlerden herhangi birine aşırı duyarlı (alerjik) olabilecek kişilerde kullanılmamalıdır. Ayrıca interstisyel pnömoni veya pulmoner fibroz (akciğer hastalıkları) olan hastalarda kullanılmamalıdır.
Vectibix neden onaylandı?
İnsan Kullanımına Yönelik Tıbbi Ürünler Komitesi (CHMP), floropirimidinler, oksaliplatin ve floropirimidin içeren kemoterapi rejimlerinin başarısızlığından sonra, salgın büyüme faktörü reseptörü (EGFR) eksprese eden metastatik kolorektal kanserli hastaların monoterapi tedavisi için Vectibix'in faydalarının risklerinden daha büyük olduğu sonucuna varmıştır. irinotekan, eğer tümörler gene sahipse KRAS değişmedi (Vahşi tip). Bu nedenle Komite, Vectibix için bir pazarlama izni verilmesini tavsiye etti.
Vectibix'e "" koşullu onay verilmiştir. Bu, ilaç hakkında, özellikle aşağıdakileri içeren tümörleri olan hastalarda güvenliği ve etkinliği ile ilgili daha fazla bilginin sunulması gerektiği anlamına gelir. KRAS değişmedi. Avrupa İlaç Ajansı (EMEA) mevcut tüm yeni bilgileri yıllık olarak gözden geçirecek ve gerekirse bu özet güncellenecektir.
Vectibix için hala hangi bilgiler bekleniyor?
Vectibix'i yapan şirket, kolorektal kanser hastalarında ilacın güvenliği ve etkinliği ile ilgili ek çalışmaların sonuçlarını sağlayacaktır. KRAS ilaç kullanan hastaların yaşam kaliteleri de değişti. Bunlar, hem geçmişte tedavi görmüş hastalarda hem de kanser tedavisi görmemiş hastalarda Vectibix'in diğer ilaçlarla kombinasyon halinde kullanımını değerlendirmeyi amaçlayan çalışmaları ve ayrıca Vectibix'in etkinliğini doğrulamayı amaçlayan bir çalışmayı içerir. Vectibix, onaylanmış dozda tek başına verilir.
Vectibix ile ilgili diğer bilgiler:
3 Aralık 2007'de Avrupa Komisyonu Amgen Europe B.V. Vectibix için Avrupa Birliği genelinde geçerli bir "Pazarlama İzni".
Vectibix EPAR'ın tam sürümü için buraya tıklayın.
Bu özetin son güncellemesi: 03-2009.
Bu sayfada yayınlanan Vectibix - panitumumab ile ilgili bilgiler güncelliğini yitirmiş veya eksik olabilir. Bu bilgilerin doğru kullanımı için Sorumluluk Reddi ve faydalı bilgiler sayfasına bakın.